
下列有关说法错误的是
A.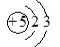 既可以表示10B的原子结构,也可以表示11B的原子结构
既可以表示10B的原子结构,也可以表示11B的原子结构
B.H++OH-=H2O既可以表示NaOH与盐酸反应,也可以表示Ba(OH)2与硫酸反应
C.CH4分子的空间结构与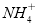 的相同
的相同
D.C2H4O2既可以表示乙酸的分子式,也可以表示甲酸甲酯的分子式
科目:高中化学 来源:2014-2015学年江苏省扬州市高三上学期期末考试化学试卷(解析版) 题型:选择题
某温度时,N2与H2反应过程中的能量变化如图所示。下列叙述正确的是
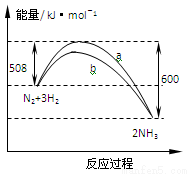
A.1 mo N2与3 mo H2充分反应可以放出92 kJ的热量
B.b曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该反应的焓变减小
D.正反应的活化能等于逆反应的活化能
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长沙市高三4月月考理综化学试卷(解析版) 题型:选择题
已知酸性:H2SO4>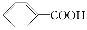 >H2CO3>
>H2CO3>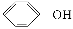 >HCO3—,综合考虑反应物的转化率和原料成本等因素,将
>HCO3—,综合考虑反应物的转化率和原料成本等因素,将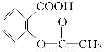 转变为
转变为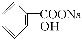 的最佳方法是
的最佳方法是
A.与足量的NaOH溶液共热后,再通入足量CO2
B.与足量的NaOH溶液共热后,再加入适量H2SO4
C.与稀H2SO4共热后,加入足量的NaOH溶液
D.与稀H2SO4共热后,加入足量的Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省西安市高三下学期二模考试理综化学试卷(解析版) 题型:选择题
化学与工农业生产和人类生活密切相关。下列说法中,不正确的是
A.使用太阳能等代替化石燃料,符合低碳节能减排的要求
B.油脂在碱性条件下水解可制得肥皂
C.海轮外壳上镶入锌块,可减缓船体的腐蚀
D.高纯度的硅单质广泛用于制作光导纤维
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南周口市高三3月教学质量监测理综化学试卷(解析版) 题型:选择题
已知A、B、C、D、E五种主族元素分别位于第1、2、3周期,原子序数依次增大,其中A与C、B与D分别同主族,且B原子的最外层电子数等于A与C原子序数之和的一半,下列叙述正确的是
A.原子半径:A<B<C<D<E
B.D、E的气态氢化物的热稳定性:D>E
C.A与B、C与B均能形成X2Y2型化合物,且其中所含有的化学键类型相同
D.另外四种元素能够分别与C形成含单原子核阴离子的离子化合物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省新校高三4月模拟化学试卷(解析版) 题型:实验题
(14分)下图是实验室用乙醇与浓硫酸和溴化钠反应来制备溴乙烷的装置,反应需要加热,图中省去了加热装置。有关数据见表:
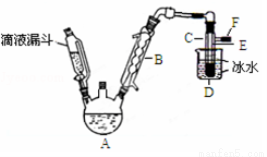
表.乙醇、溴乙烷、溴有关参数
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色液体 | 无色液体 | 深红棕色液体 |
密度/gcm-3 | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
(1)制备操作中,加入的浓硫酸必需进行稀释,其目的是 (选填序号)。
a.减少副产物烯和醚的生成
b.减少Br2的生成
c.减少HBr的挥发
d.水是反应的催化剂
(2)已知加热温度较低时NaBr与硫酸反应生成NaHSO4,写出加热时A中发生的主要反应的化学方程式 。
(3)仪器B的名称 ,冷却水应从B的 (填“上”或“下”)口流进。
(4)反应生成的溴乙烷应在 中(填“A”或“C”中)。
(5)若用浓的硫酸进行实验时,得到的溴乙烷呈棕黄色,最好选择下列 (选填序号)溶液来洗涤产品。
a.氢氧化钠 b.亚硫酸钠 c.碘化亚铁 d.碳酸氢钠
洗涤产品时所需要的玻璃仪器有 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省新校高三4月模拟化学试卷(解析版) 题型:选择题
下列化学用语书写正确的是
A.次氯酸的结构式:H—Cl—O
B.丙烷分子的球棍模型示意图:
C.NH4H的电子式: 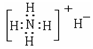
D.S2-的结构示意图:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省黄山市高三毕业班第二次质量检测理综化学试卷(解析版) 题型:简答题
(14分)下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系。请回答下列问题:

(1)Y在元素周期表中位于第____周期、第 族;P的基态原子核外电子排布式为________。
(2)Y、P、R第一电离能大小的顺序为 (用化学符号表示,下同),X、R、W的气态氢化物水溶液酸性大小顺序为 。
(3)X、Z的单质按物质的量比1:2反应生成的化合物中化学键类型有 ;计算2mol该化合物与标准状况下33. 6LCO2和l0mol水蒸气混合物充分反应后转移电子的物质的量是 。
(4)Q单质与Z的最高价氧化物对应水化物的浓溶液反应,化学方程式为 。
(5)已知:反应I CaSO4( s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H=+218.4kJ/mol
CaO(s)+SO2(g)+CO2(g) △H=+218.4kJ/mol
反应Ⅱ CaSO4(s)+4CO(g) CaS(s)+4CO2(g) △H=-175.6kJ/mol
CaS(s)+4CO2(g) △H=-175.6kJ/mol
假设某温度下,反应I的速率(v1)大于反应II的速率(v2),则下列反应过程能量变化示意图正确的是

查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省台州市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列关于化学的叙述中,错误的是
A.在化工生产中应遵循“绿色化学”的思想
B.通常用来衡量一个国家的石油化学工业发展水平的标志是乙烯的产量
C.在元素周期表的金属和非金属分界线附近寻找半导体材料
D.根据元素周期律,由HClO4可以类推出氟元素也存在最高价氧化物的水化物HFO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com