
【题目】甲酸香叶酯是一种食品香料,可以由香叶醇与甲酸发生酯化反应制得。下列说法正确的是( )
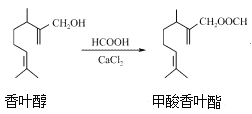
A. 香叶醇的分子式为C11H18O
B. 香叶醇在浓硫酸、加热条件下可发生消去反应
C. 香叶醇与CH2=CHCH=CHCH2OH互为同系物
D. 香叶醇与甲酸香叶酯均不能发生银镜反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】过氧化氢(H2O2)的水溶液俗称双氧水。双氧水常被称为化学反应中的“绿色试剂”。已知,在含少量I-的溶液中,H2O2会较快分解,反应如下:反应①:H2O2+I- → H2O+IO-; 反应②:H2O2+IO- → H2O+O2+I-,完成下列填空:
(1)反应①中的氧化产物是_________,被还原的元素是___________。
(2)标出反应②中电子转移的方向和数目。_______________
(3)H2O2分解过程中,I-的作用是__________。
(4)根据反应①和反应②,请说明双氧水被称为“绿色试剂”的主要原因是_____。
(5)H2O2是一种二元弱酸,写出第一步电离的电离方程式:________,双氧水可漂白纤维织物,目前认为是其中过氧化氢离子(HOO-)的作用。为了增强其漂白效果,应选择在____(填“酸”、“碱”或“中”)性条件下进行。
(6)向盐酸酸化的FeCl2溶液中加入双氧水,溶液由浅绿色变为棕黄色,写出该变化的化学反应方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水综合利用要符合可持续发展的原则,其联合工业体系(部分)如图所示,下列说法错误的是
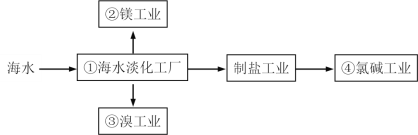
A.①中可采用蒸馏法B.②中可通过电解法制金属镁
C.③中提溴涉及到复分解反应D.④的产品可生产盐酸、漂白液等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是重要的化工原料,可以制得多种有机制品。用乙炔为原料制备PI(聚异戊二烯)的流程如图:
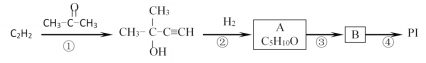
(1)有机物A中官能团的名称___,反应③的反应条件____。
(2)若将①中反应物“![]() ”改为“乙醛”,经过②③④后得到产物的结构简式是__。
”改为“乙醛”,经过②③④后得到产物的结构简式是__。
乙炔在一定条件下还可合成PVB塑料(聚乙烯醇缩丁醛):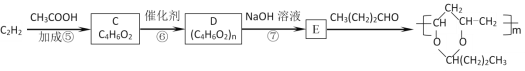
已知:-CHO+ +H2O
+H2O
(3)写出C的结构简式为__;2分子乙炔也能发生加成反应得到链烃,其反应产物的结构简式为___。
(4)反应⑦的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校研究性学习小组用相同大小的铜片和锌片为电极研究水果电池,得到的数据如下表所示:

实验编号 | 水果种类 | 电极间距离/cm | 电流大小/μA |
① | 西红柿 | 1 | 98.7 |
② | 西红柿 | 2 | 72.5 |
③ | 苹果 | 2 | 27.2 |
(1)该实验的目的是探究水果种类和________对水果电池电流大小的影响。
(2)上图所示的装置中,做负极的材料是______(填“锌片”或“铜片”),该装置给将_________转变为电能。
(3)能表明水果种类对电流大小有影响的实验编号是____和_______。
(4)请你再提一个可能影响水果电池电流大小的因素:______________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸是一种重要的化工原料,工业上采用氨催化氧化法制备,生产过程中发生的反应有:
NH3(g)+![]() O2(g)
O2(g)![]() NO(g)+
NO(g)+![]() H2O(l) △H1= -292.3kJ/mol
H2O(l) △H1= -292.3kJ/mol
NO(g)+![]() O2(g)= NO2(g) △H2= -57.1kJ/mol
O2(g)= NO2(g) △H2= -57.1kJ/mol
3NO2(g)+ H2O(l)=2HNO3(aq)+NO(g) △H3= -71.7kJ/mol
回答以下问题:
(1) NH3(g)+2O2(g)=HNO3(aq)+ H2O(l) 的 △H= ___________ kJ/mol。原料气体(NH3、O2)在进入反应装置之前,必须进行脱硫处理。其原因是____。
(2)研究表明2NO(g)+ O2(g)![]() 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
(a)2NO(g)![]() N2O2(g)(快) (b)N2O2(g)+ O2(g)
N2O2(g)(快) (b)N2O2(g)+ O2(g)![]() 2NO2(g)(慢)
2NO2(g)(慢)
①该反应的速率由b步决定,说明b步反应的活化能比a步的 ___(填“大”或“小”)。
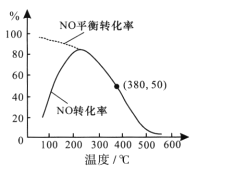
②在恒容条件下,NO和O2的起始浓度之比为2:1,反应经历相同时间,测得不同温度下NO转化为NO2的转化率如图,则150℃时,v正___ v逆(填“>”或“<”)。若起始c(O2)=5.0×10-4mol/L,则380℃下反应达平衡时c(O2)=____mol/L。
(3) T1温度时,在容积为2L的恒容密闭容器中发生反应2NO+ O2![]() 2NO2,实验测得:v正=v(NO)消耗=2v(O2)消耗=k正c2(NO)·c(O2),v逆=v(NO2)消耗=k逆c2(NO2),k正、k逆为速率常数,受温度影响。容器中各反应物和生成物的物质的量随时间变化如下图所示:
2NO2,实验测得:v正=v(NO)消耗=2v(O2)消耗=k正c2(NO)·c(O2),v逆=v(NO2)消耗=k逆c2(NO2),k正、k逆为速率常数,受温度影响。容器中各反应物和生成物的物质的量随时间变化如下图所示:
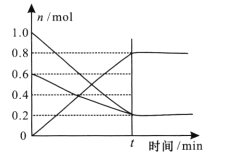
①下列说法能表明该反应已经达到平衡状态的是 ____填序号)
A. 混合气体的密度不变 B. 混合气体的颜色不变
C. k正、k逆不变 D. 2v正(O2)=v逆(NO2)
②化学平衡常数K与速率常数k正、k逆的数学关系式K=____。
③温度为T1时的化学平衡常数K= _____。若将容器的温度变为T2时,k正=k逆,则T2 ___T1(填“>
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是
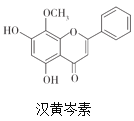
A. 能与Na2CO3溶液反应放出气体
B. 该物质遇FeCl3溶液不显色
C. 1mol该物质与溴水反应,最多消耗2molBr2
D. 与足量H2发生加成反应后,该分子中官能团的种类减少1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的离子方程式书写不正确的是
A. 用FeCl3溶液腐蚀印刷线路板上的Cu:2Fe3++Cu=2Fe2++Cu2+
B. 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑
C. 稀硝酸中加入过量铁粉: Fe+4H++NO3-=Fe3++NO↑+2H2O
D. 用Na2CO3溶液浸泡锅炉水垢:CaSO4(s)+CO32-(aq)![]() CaCO3(s)+SO42-(aq)
CaCO3(s)+SO42-(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)等物质的量的CO与CO2之间:二者的质量之比为______,所含氧原子数之比为______。
(2)在标准状况下,CO和CO2混合气体的质量为32g,体积为22.4L,则混合气体中CO的体积为______, CO2的质量为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com