
【题目】下列实验仪器不宜直接用来加热的是( )
A. 试管 B. 坩埚 C. 蒸发皿 D. 烧杯
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. HF、HCl、HBr、HI的熔沸点依次升高
B. N2与CO互为等电子体,具有相似的空间结构
C. 乙醇分子与水分子之间只存在范德华力
D. 氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤化工中常需研究不同温度下平衡常数、投料比及产率等问题。
已知:CO(g)+H2O(g)![]() H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:
温度/℃ | 400 | 500 | 830 | 1 000 |
平衡常数K | 10 | 9 | 1 | 0.6 |
试回答下列问题:
(1)上述反应平衡常数的表达式为 _____________,正反应是___________反应(填“放热”或“吸热”)。
(2)某温度下,上述反应达到平衡后,保持容器体积不变升高温度,正反应速率___________(填“增大”“减小”或“不变”),容器内混合气体的压强________ (填“增大”“减小”或“不变”)。
(3)830 ℃时,在恒容反应器中发生上述反应,按下表中的物质的量投入反应混合物,其中向正反应方向进行的有 _________ (选填字母)。
A | B | C | D | |
n(CO2)/mol | 3 | 1 | 0 | 1 |
n(H2)/mol | 2 | 1 | 0 | 1 |
n(CO)/mol | 1 | 2 | 3 | 0.5 |
n(H2O)/mol | 5 | 2 | 3 | 2 |
(4)830 ℃时,在2 L的密闭容器中加入4 mol CO(g)和6 mol H2O(g)达到平衡时,CO的转化率是 ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol/L稀氨水加水稀释,下列说法正确的是( )
A. 溶液中c(H+)和c(OH-)都减小 B. 溶液中c(H+)增大
C. NH3·H2O电离平衡向左移动 D. 溶液pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是 ( )
A. 1mol任何物质都含有6.02×1023个原子
B. 0.012kg12C 含有阿伏加德罗常数个碳原子
C. 在使用摩尔表示物质的量的单位时,应指明粒子的种类
D. 物质的量是国际单位制中七个基本物理量之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电化学腐蚀及防护的装置如右图所示。下列有关说法错误的是( )
A.d为石墨,铁片腐蚀加快
B.d为石墨,石墨上电极反应为:O2 + 2H2O + 4e → 4OH–
C.d为锌块,铁片不易被腐蚀
D.d为锌块,铁片上电极反应为:2H+ + 2e → H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列物质在水溶液中的电离方程式:
①Ba(OH)2: ;
②NaHSO4: ;
③写出①②水溶液混合后恰好沉淀完全的离子方程式______________________
(2)砷及其化合物有毒,如砒霜(As2O3)有剧毒,环境监测和法医学分析砒霜中毒的反应原理:As2O3+6Zn+12HCl=6ZnCl2+2AsH3↑+3H2O,①反应中还原剂是 ,被还原的元素是 ,(用化学式回答)若参加反应Zn的质量为19.5g,则生成的气体在标准状况下的体积为_________L,
②用双线桥法标出上述反应中电子转移的方向和数目。
(3)实验室里需要纯净的NaCl溶液,但手边只有混有Na2SO4、NH4HCO3的NaCl.某学生设计了如图所示方案提取纯净的NaCl溶液.(已知:NH4HCO3![]() NH3↑+CO2↑+H2O)
NH3↑+CO2↑+H2O)
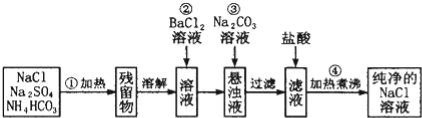
①150℃时,一定量的NH4HCO3完全分解后所得气体的平均相对分子质量为 (保留至小数点后一位).
②操作③所得到的悬浊液与胶体的本质区别是 .
③进行操作②后,判断SO42﹣是否已除尽方法是 .
④操作②加BaCl2溶液后生成沉淀,不必进行过滤就可进行操作③加碳酸钠溶液,其理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 氯气和明矾都能用于自来水的杀菌消毒
B. 常温下,浓硫酸和浓硝酸都能用铜制容器盛装
C. 钢铁设备连接锌块或电源正极都可防止其腐蚀
D. 酸雨主要是由人为排放的硫氧化物和氮氧化物等转化而成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com