
科学家最近在-100℃的低温下合成一种烃X,此分子的模型如右图
(图中的连线表示化学键),下列说法正确的是( )
A.X能使溴的四氯化碳溶液褪色
B.X是一种在常温下能稳定存在的液态烃
C.X分子中在同一平面上的碳原子最多有5个
D.充分燃烧等质量的X和甲烷,X消耗氧气多

 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
某研究性学习小组计划研究当地酸雨的形成过程,于是取来雨水作水样进行测定,随时间的推移,多次测定该样品的pH,得到如下数据:
| 时间(h) | 开始 | 8 | 16 | 24 | 32 | 40 | 48 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(1)雨水样品放置时pH变化的主要原因为______________________________________
(用化学方程式表示 )。由此可以得出酸雨的形成过程可能是_______________________。
)。由此可以得出酸雨的形成过程可能是_______________________。
如果将刚取样的上述雨水和自来水相混合,pH将______(填“增大”、“减小”或“不变”),原因是________________________ __________________________________,
__________________________________,
二氧化硫表现________性。
(2)下面是酸雨给人类造成的危害,其中不正确的是___________________________。
A.腐蚀建筑物、雕塑等 B.污染水源
C.改良碱性土壤 D.损害庄稼
(3)你认为减少酸雨产生的途径可采取的措施是_____________________________。
①少用煤作燃料 ②把工厂的烟囱造高 ③燃料脱硫
④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤
C.①③⑤ D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
已知4NH3(g)+5O2(g) 4NO(g)+6H2O(g)△H<0,下列有关叙述正确的( )A.上述反应的化学反应速率关系:2 v(NH3)=3 v(H2O)
4NO(g)+6H2O(g)△H<0,下列有关叙述正确的( )A.上述反应的化学反应速率关系:2 v(NH3)=3 v(H2O)
B.若在2L的密闭容器中反应,经过3min后NH3的物质的量由10mol变为7mol
则v (NH3)=0.5mol·L-1·s-1
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.若降低温度,反应速率将会减小且平衡将被破坏
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.分子式为C4H8有机物最多存在4个C—C单键
B.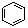 和
和  均是芳香烃,
均是芳香烃, 既是芳香烃又是芳香化合物
既是芳香烃又是芳香化合物
C. 和
和 分子组成相差一个—CH2—,因此是同系物关系
分子组成相差一个—CH2—,因此是同系物关系
D.分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此可以初步推测有机物结构简式为C2H5-OH
查看答案和解析>>
科目:高中化学 来源: 题型:
两种气态烃的混合物共1 L,在空气中完全燃烧得到1.5 L CO2和2 L水蒸气(体积均在同温同压下测定),关于此混合烃的判断正确的是 ( )
A.肯定是甲烷和乙烯的混合物 B.一定不是甲烷和乙烯的混合物
C.一定含乙烯,不含甲烷 D.两种烃分子中氢原子数都是4
查看答案和解析>>
科目:高中化学 来源: 题型:
二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料。以CH4和
H2O为原料制备二甲醚和甲醇的工业流程如下:

请填空:
(1)一定条件下,反应室1中发生反应CH4(g)+H2O(g) CO(g)+3H2(g) ΔH>0。
CO(g)+3H2(g) ΔH>0。
其它条件不变,只降低温度,逆反应速率将 (填“增大”、“减小”或“不变”)。
 (2)反应室3(容积可变的密闭容器)中 0.2molCO与
(2)反应室3(容积可变的密闭容器)中 0.2molCO与
0.4molH2在催化剂作用下发生可逆反应生成甲醇:
CO(g)+2H2(g) CH3OH(g),CO的平衡转化率
CH3OH(g),CO的平衡转化率
与温度、压强的关系如右图所示,则:
①P1 P2 (填“<”、“>”或“=”)。
②在压强P1下,100℃时反应达到化学平衡,反应室3的容积变为2L,此时 若温度不变,再加入1.0molCO后重新达到平衡,CO的平衡转化率 (填“增大”、“不变”或“减小”)。
③保持容积为2L不变,温度100℃不变,向反应室3中再通入0.2molCO与0.4molH2, CO的平衡转化率 (填“增大”、“不变”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于原子结构的叙述正确的是 ( )
A.所有的原子核都是由质子和中子组成的
B.原子的最外层电子数不超过8个(除K层)
C.稀有气体原子的最外层电子数均为8
D.M层最多容纳的电子数为32个
查看答案和解析>>
科目:高中化学 来源: 题型:
海洋植物如海带海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋中提取碘的流程如下:
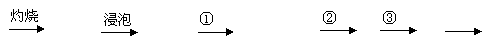 |
海藻 海藻灰 悬浊液 含I-的溶液 X Y 碘
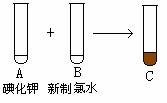
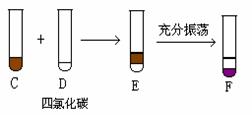 某化学兴趣小组将上述流程②③设计如下图:
某化学兴趣小组将上述流程②③设计如下图:
② ③
回答下列问题:
(1)写出提取过程①③中实验操作名称:① ③ 。
(2)写出过程②中有关反应的离子方程式:_____________________________________。
(3)过程③的F的下层液体的颜色为_____色,上层液体中溶质的主要成分为_________。
(4) 在灼烧过程中,将使用到的(除泥三角外)硅酸盐质实验仪器有________________(填代号,限填两项)。
A.试管 B.瓷坩埚 C.坩埚钳 D.铁三角架 E.酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.某兴趣小组用如图装置做了两次实验。
实验①:向甲池的Pt电极表面通氢气,发现电流计指针发生了偏转,乙池的Pt电极表面出现气泡。
实验②:向乙池的Pt电极表面通氧气,发现电流计指针也发生了偏转,且偏转方向与实验①相同,同时甲池的Pt电极表面也出现气泡。

(1)实验①,甲池通氢气的Pt电极为________________极,电极反应式为_________________________________________________。
(2)实验②,乙池通氧气的Pt电极为________________极,电极反应式为__________________________________________________。
(3)两次实验中原电池的总反应相同,总反应的离子方程式为___
__________________________________________________________。

Ⅱ.电解法污水处理技术已很成熟。富含悬浮物的工业污水采用如图装置进行处理:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,吸附部分悬浮物沉降,同时阴极产生的气泡将部分悬浮物带到水面形成浮渣层,然后滤去沉淀、撇掉浮渣层。富含有机废物的生活污水也可用同样方法进行处理。污水中的有机废物能被阳极的某一产物迅速降解成二氧化碳、水等无机物。
(1)在电解处理过程中,若污水中离子浓度较小,导电能力较差,处理效率下降,此时可向污水中加入适量的________。
a.BaSO4 b.CH3COOH
c.NaNO3 d.CH3OH
(2)电解处理过程中,阳极实际发生了两个电极反应,阳极的电极反应式分别是①________________;②________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com