
【题目】资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学设计了如下实验方案并验证产物、探究反应原理。
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能为_________;
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
实验序号 | 实验 | 实验现象 | 结论 |
实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体成分为___①______ |
实验Ⅲ | 取实验Ⅰ中的白色不溶物,洗涤,加入足量____②_____ | _____③____ | 白色不溶物可能含有猜测2中不溶物 |
实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 产生白色沉淀 | 溶液中存在 _____④____ |
(3)为进一步确定实验1的产物,设计定量实验方案,如图所示:

称取实验1中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部通入装置A和B中.实验后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式:_________;(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡和白色不溶物的原因:_________。
【答案】
(1)Mg(OH)2 ;
(2)氢气;稀盐酸;产生气泡沉淀全部溶解;CO32-;
(3)Mg(OH)2(CO3)2或2MgCO3Mg(OH)2 ;
(4)NaHCO3溶液中存在平衡,HCO3-H++CO32-、H2OH++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)22MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行。
【解析】
试题分析:(1)依据猜测可知白色不溶物可能是Mg(OH)2 或MgCO3或Mg(OH)2 ,MgCO3,故答案为:Mg(OH)2 ;
(2)迅速反应,产生大量气泡和白色不溶物,可以说明镁与饱和碳酸氢钠溶液反应能生成一种无色气体和一种白色不溶物;气体安静燃烧、产生淡蓝色火焰,说明该气体具有可燃性,再根据质量守恒定律反应前后元素种类不变,该气体可能是氢气或一氧化碳,如果测定是一氧化碳时,燃烧后需要用到澄清石灰水,所以该气体是氢气;依据实验Ⅲ的推断分析,加入一种试剂产生气泡可知碳酸盐与酸反应产生二氧化碳,所以加入的是酸,有气泡产生,说明含有碳酸镁;加入盐酸沉淀碳酸镁全部溶解;依据实验Ⅳ加入氯化钙生成沉淀证明含有碳酸根离子,故答案为:氢气;稀盐酸;产生气泡沉淀全部溶解;CO32-;
(3)B中碱石灰质量的增加量就是生成的二氧化碳的质量,所以生成二氧化碳的质量为8.8g,设生成8.8g二氧化碳,需要碳酸镁的质量为x则:
MgCO3+2HCl═MgCl2+H2O+CO2↑
84 44
x 8.8g
根据:![]() =
=![]() ,解得x=16.8g,所以含有氢氧化镁质量为:22.6g-16.8g=5.8g;碳酸镁和氢氧化镁物质的量之比为:
,解得x=16.8g,所以含有氢氧化镁质量为:22.6g-16.8g=5.8g;碳酸镁和氢氧化镁物质的量之比为:![]() :
:![]() =0.2:0.1=2:1,白色不溶物的化学式为Mg(OH)2(CO3)2或2MgCO3Mg(OH)2,故答案为:Mg(OH)2(CO3)2或2MgCO3Mg(OH)2 ;
=0.2:0.1=2:1,白色不溶物的化学式为Mg(OH)2(CO3)2或2MgCO3Mg(OH)2,故答案为:Mg(OH)2(CO3)2或2MgCO3Mg(OH)2 ;
(4)NaHCO3溶液中存在平衡,HCO3-![]() H++CO32-、H2O
H++CO32-、H2O![]() H++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)22MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行,故答案为:NaHCO3溶液中存在平衡,HCO3-
H++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)22MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行,故答案为:NaHCO3溶液中存在平衡,HCO3-![]() H++CO32-、H2O
H++CO32-、H2O![]() H++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)22MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行。
H++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)22MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在一密闭容器中充入2mol HI气体,发生反应:2HI(g) ![]() H2(g)+I2(g) ΔH>0 ,达到化学平衡状态后,为使体系颜色加深,可采取的措施是( )
H2(g)+I2(g) ΔH>0 ,达到化学平衡状态后,为使体系颜色加深,可采取的措施是( )
①维持温度和容器体积不变,再充入少量I2(g) ②维持温度和压强不变,再充入2molHI ③降低温度 ④加压(缩小容器体积) ⑤升高温度
A.①④⑤B.②③C.②③④D.①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国电池的年市场消费量约为80亿只,其中![]() 是锌锰干电池,利用废旧锌锰干电池制备硫酸锌晶体
是锌锰干电池,利用废旧锌锰干电池制备硫酸锌晶体![]() 和纯
和纯![]() 的工艺如下图所示:
的工艺如下图所示:
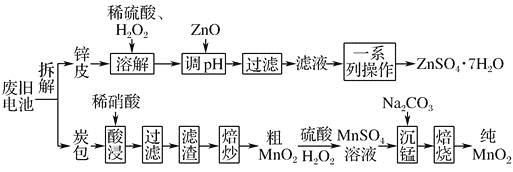
已知:
①锌皮的主要成分为Zn,含有少量Fe;炭包的主要成分为![]() 、
、![]() 、
、![]() 、碳粉等,还含有少量的Cu、Ag、Fe等。
、碳粉等,还含有少量的Cu、Ag、Fe等。
②![]() ;
;![]() ;
;![]() 。
。
(1)除去炭包中碳粉的操作为________。
A.酸浸 ![]() 过滤
过滤 ![]() 焙炒
焙炒 ![]() 焙烧
焙烧
(2)粗![]() 转化为
转化为![]() 时,主要反应的离子方程式为____________________________。
时,主要反应的离子方程式为____________________________。
(3)焙烧时发生反应的化学方程式为__________________________________________。
(4)制备硫酸锌晶体流程中,在溶解时加![]() 的作用是____________________________,用ZnO调节溶液pH的目的是_____________________________。滤液制备硫酸锌晶体
的作用是____________________________,用ZnO调节溶液pH的目的是_____________________________。滤液制备硫酸锌晶体![]() 的一系列操作为:____________、____________、________、洗涤、干燥。
的一系列操作为:____________、____________、________、洗涤、干燥。
(5)“草酸钠![]() 高锰酸钾返滴法”可测定
高锰酸钾返滴法”可测定![]() 的纯度,取
的纯度,取![]() 样品于锥形瓶中,加入适量稀硫酸,再加入足量的
样品于锥形瓶中,加入适量稀硫酸,再加入足量的![]() 溶液,最后用
溶液,最后用![]() 溶液滴定剩余的
溶液滴定剩余的![]() 。其中
。其中![]() 与
与![]() 溶液反应的离子方程式为__________________________________________。
溶液反应的离子方程式为__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学的应用十分广泛,在分析检测、有机合成等领域应用很广,请分析下列几种电化学装置并回答问题:

(1)肼(N2H4)又称联氨,可作燃料电池的燃料。肼燃料电池的原理如图 1 所示,正极上发生反应的电极反应式为___________________________________________;在肼燃料电池使用过程中,负极区的pH_____________(填写“增大”、“减小”或“不变”)。

(2)某模拟“人工树叶”的电化学实验装置如图2所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。该装置工作时,H+从____________(填字母,后同)极区向____________极区迁移,将电能转化为___________能,每生成3molO2,有______________gCO2被还原。
(3)图3中甲装置为C3H8O的燃料电池(电解质溶液为KOH溶液)装置,该同学想在乙装置中实现铁上镀铜,则f处通________________________________,写出电极c上的电极反应式:__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组有机化合物中,不论两者以什么比例混合,只要总物质的量一定,则完全燃烧时生成的水的质量和消耗氧气的质量不变的是
A. CH4O,C3H4O5B. C3H6,C3H8O
C. C3H8,C4H6D. C2H6,C4H6O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)铅是碳的同族元素,比碳多4个电子层。铅在元素周期表的位置为第____周期.第___族;PbO2的酸性比CO2的酸性_____(填“强”或“弱”)。
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为_________________________________。
(3)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为___________________________;PbO2也可以通过石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生反应的电极反应式为________________,阴极上观察到的现象是_______________;若电解液中不加入Cu(NO3)2,阴极发生的电极反应式为______________________,这样做的主要缺点是__________________。
(4)PbO2在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的a点为样品失重的4.0%(即样品起始质量—a点固体质量/样品起始质量×100%)的残留固体。若a点固体组成表示为PbOx或mPbO2·nPbO,列式计算x值和m:n值_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量氨基甲酸铵![]() 加入密闭容器中,发生反应
加入密闭容器中,发生反应![]() 。该反应的平衡常数的负对数
。该反应的平衡常数的负对数![]() K
K![]() 值随温度
值随温度![]() T
T![]() 的变化曲线如图所示,下列说法错误的是
的变化曲线如图所示,下列说法错误的是
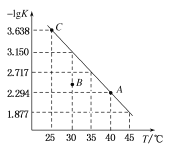
A.C点对应状态的平衡常数 K( C )![]()
B.该反应的![]() H
H ![]()
C.![]() 的体积分数不变时,该反应一定达到平衡状态
的体积分数不变时,该反应一定达到平衡状态
D.30℃时, B点对应状态的 v![]() 正
正![]() v
v![]() 逆
逆![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2NO2(红棕色)![]() N2O4(无色)△H<0。将一定量的NO2充入注射器中并密封,改变活塞位置的过程中,气体透光率随时间的变化如图所示(气体颜色越深,透光率越小)。下列说法不正确的是( )
N2O4(无色)△H<0。将一定量的NO2充入注射器中并密封,改变活塞位置的过程中,气体透光率随时间的变化如图所示(气体颜色越深,透光率越小)。下列说法不正确的是( )

A. b点达到平衡状态
B. b点与a点相比,c(NO2)、c(N2O4)均减小
C. d点:v(正)<v(逆)
D. 若在c点将温度降低,其透光率将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Geliening 是治疗白血病和多种癌症的一种抗癌药物,在其合成过程中的一种中间产物结构表 示如图,下列有关该中间产物的说法不正确的是( )
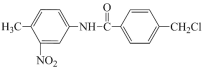
A.分子中含有3种官能团
B.该物质的分子式为C15H13O3N2Cl
C.该分子中最多有15 个碳原子共平面
D.1mol该物质可与1molNaOH发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com