
某溶液,只可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、NO2-、CO32-、NO3-,现取两份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有5.84g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.1g;
②将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀1.0g,该沉淀能溶于稀盐酸产生无色气体;
③第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,用50mL0.5mol·L-1的硫酸溶液恰好完全吸收,酸也不剩余。
根据上述实验,以下推测不正确的是( )
A.原溶液一定不存在较大浓度的H+、Mg2+
B.原溶液确定含NH4+、NO2-、CO32-,且物质的量之比为5︰2︰1
C.不能确定原溶液是否含有K+、NO3-
D.实验中产生的棕色气体遇空气颜色会加深
C
【解析】
试题分析:第一份加足量AgNO3溶液后,有5.84g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.1g,这说明该白色沉淀中一定含有亚硝酸银,亚硝酸银与盐酸反应生成氯化银与亚硝酸,亚硝酸不稳定分解生成NO、NO2和水。所以原溶液中一定含有NO2-,则氢离子一定不能大量共存。将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀1.0g,该沉淀能溶于稀盐酸产生无色气体,则该白色沉淀应该是碳酸钙,物质的量是0.01mol,所以气体中含有CO2,这说明反应①中生成的白色沉淀一定有碳酸银,则原溶液中一定含有CO32-。因此Mg2+就一定不能大量共存。根据碳原子守恒,CO32-的物质的量是0.01mol。5.84g沉淀中亚硝酸银沉淀的质量=5.84g-0.01mol×276g/mol=3.08g,因此亚硝酸银的物质的量=3.08g÷154g/mol=0.02mol,则原溶液中NO2-的物质的量是0.02mol。第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,该气体一定是氨气,因此原溶液中含有NH4+。用50mL0.5mol/L的硫酸溶液恰好完全吸收,酸也不剩余,硫酸的物质的量是0.025mol,则氨气的物质的量是0.025mol×2=0.05mol,则原溶液中NH4+的物质的量是0.05mol,所以原溶液确定含NH4+、NO2-、CO32-,且物质的量之比为5︰2︰1,因此选项A、B正确。根据电荷守恒可知,原溶液中一定还含有NO3-,但K+不能确定,C不正确;实验中产生的棕色气体中含有NO,遇空气生成红棕色NO2,所以颜色会加深,D正确,答案选C。
考点:考查考查离子共存、离子检验的有关判断


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 预期现象和结论 |
| 步骤1:将菠菜研磨后,浸泡、过滤得到澄清待测溶液. | |
| 步骤2:调节溶液至弱碱性,滴加足量CaCl2溶液. | 出现白色沉淀,说明菠菜中可能含有草酸盐和碳酸盐. |
| 步骤3:取步骤2的沉淀于试管中, 加入足量1 mol?L-1 HCl,将产生的气体通入足量澄清石灰水中. 加入足量1 mol?L-1 HCl,将产生的气体通入足量澄清石灰水中. |
沉淀溶解,澄清石灰水变浑浊,说明菠菜中含有碳酸盐. 沉淀溶解,澄清石灰水变浑浊,说明菠菜中含有碳酸盐. |
| 步骤4: 向步骤3得到的溶液中滴加几滴0.01 mol?L-1 KMnO4. 向步骤3得到的溶液中滴加几滴0.01 mol?L-1 KMnO4. |
溶液紫红色褪去,说明菠菜中含有草酸盐. 溶液紫红色褪去,说明菠菜中含有草酸盐. |
| 0.0100mol/L×V×10-3L×5×100mL×88g/mol |
| 2×25mL×mg |
| 0.0100mol/L×V×10-3L×5×100mL×88g/mol |
| 2×25mL×mg |
查看答案和解析>>
科目:高中化学 来源: 题型:
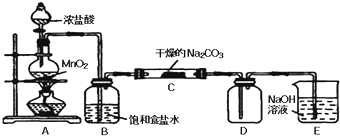
| 实验步骤 | 预期现象和结论 |
| 步骤1:取C中的少量固体样品于试管中,加入蒸馏水至固体溶解,然后各取1~2mL所得溶液分别置于甲、乙两支试管中. | 得到无色溶液 |
| 步骤2:向甲试管中加入过量的BaCl2溶液,静置 | 若溶液变浑浊,证明固体中含碳酸钠. |
| 步骤3: |
|
| 步骤4: |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省揭阳市高三第一次高考模拟考试理综化学试卷(解析版) 题型:实验题
某同学从报刊上了解到菠菜中富含可溶性草酸盐和碳酸盐,决定用实验验证这一事实并检测草酸盐含量。进一步查阅资料得知,草酸(H2C2O4)是酸性强于醋酸的二元有机酸,还是一种还原性较强的物质,如2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O,草酸钙(CaC2O4)不溶于水和醋酸,能溶于强酸:CaC2O4+2H+= H2C2O4+Ca2+。
(1)设计实验方案验证菠菜中含有草酸盐和碳酸盐,补充完成实验步骤、预期现象和结论。
限选试剂:1 mol·L-1 H2SO4、1 mol·L-1 HCl、0.1 mol·L-1 NaOH、1 mol·L-1 CaCl2、0.01 mol·L-1 KMnO4、澄清石灰水。
|
实验步骤 |
预期现象和结论 |
|
步骤1:将菠菜研磨后,浸泡、过滤得到澄清待测溶液。 |
|
|
步骤2:调节溶液至弱碱性,滴加足量CaCl2溶液。 |
出现白色沉淀,说明菠菜中可能含有草酸盐和碳酸盐。 |
|
步骤3:取步骤2的沉淀于试管中,
|
|
|
步骤4:
|
|
(2)要准确测定菠菜中草酸盐含量,请回答有关问题:
① 操作:取m g菠菜样品,将其中草酸盐转化为CaC2O4沉淀分离出来,用盐酸溶解后,将溶液转入_________中加水配制成100mL溶液。每次用_____________移取25.00mL该溶液,用0.0100mol·L-1 KMnO4标准溶液滴定,平均消耗标准溶液V mL。
② 计算:菠菜中草酸盐(以C2O42-计)的质量分数为___________________。(只列式不计算。C2O42-的化学式量为88)
③ 讨论:用标准KMnO4溶液直接滴定菠菜研磨、浸泡、过滤得到的溶液,结果可能偏高,原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤 | 预期现象和结论 |
| 步骤1:将菠菜研磨后,浸泡、过滤得到澄清待测溶液. | |
| 步骤2:调节溶液至弱碱性,滴加足量CaCl2溶液. | 出现白色沉淀,说明菠菜中可能含有草酸盐和碳酸盐. |
| 步骤3:取步骤2的沉淀于试管中,______ | ______ |
| 步骤4:______ | ______ |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省如皋中学高二上学期质量检测化学试卷(必修) 题型:填空题
某盐溶液中可能含有NH4+、Ba2+、Na+、Fe2+、Cl—、CO32—、NO3—七种离子中的数种。某同学取4份此溶液样品,分别进行了如下实验:(硝酸具有强氧化性,可以氧化Fe2+、I-、S2-、SO32—等等)
①用pH试纸测得溶液呈强酸性;
②加入 过量NaOH溶液,产生有刺激性气味的气体且有沉淀生成;
过量NaOH溶液,产生有刺激性气味的气体且有沉淀生成;
③加入硝酸酸化的AgNO3溶液产生白色沉淀;
④加足量BaCl2溶液,没有沉淀产生,在溶液中加入氯水,再滴加KSCN溶液,显红色
该同学最终确定在上述七种离子中肯定含有NH4+、Fe2+、Cl—三种离子。
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
A.①②④ B.①② C.①②③④ D.②③④
(1)(3分)食品和药品关系人的生存和健康。
①市场上销售的食盐品种很多。下列食盐中,所添加的元素不属于人体必需微量元素的是 (填字母)。
A.加锌盐 B.加碘盐 C.加钙盐
②纤维素被称为“第七营养素”。食物中的纤维素虽然不能为人体提供能量,但能促进肠道蠕动、吸附排出有害物质。从化学成分看,纤维素是一种 (填字母)。
A.多糖 B.蛋白质 C.脂肪
③某同学感冒发烧,他可服用下列哪种药品进行治疗 (填字母)。
A.麻黄碱 B.阿司匹林 C.抗酸药
(2)(5分)材料是人类赖以生存和发展的重要物质基础。
①生产硅酸盐水泥和普通玻璃都需用到的共同的主要原料是 。
②生活中有大量的铝制品。 家用铝锅不能经常用热碱水洗涤去污,原因是(用离子方程式表示) 。
家用铝锅不能经常用热碱水洗涤去污,原因是(用离子方程式表示) 。
③有机玻璃受热时会软化, 易于加工成型。有机玻璃是一种 材料(选填“硅酸盐”或“纤维”或“塑料”)。导电塑料的结构可表示为
易于加工成型。有机玻璃是一种 材料(选填“硅酸盐”或“纤维”或“塑料”)。导电塑料的结构可表示为 ,则其单体的结构简式为 。
,则其单体的结构简式为 。
(3)(7分)保护环境、保护地球是人类共同的呼声。
①向煤中加入石灰石作为脱硫剂,可以减少煤燃烧时产生的SO2。发生反应的化学方程式为 。
②天然水中含有的细小悬浮颗粒可以用 做混凝剂(写名称)进行净化处理。工业废水中含有的Cr3+离子,可用熟石灰作沉淀剂,在pH为8~9时生成沉淀而除去,该反应的离子方程式是 。
③城市餐饮业会产生大量污染环境的“地沟油”。“地沟油”的主要成分是油脂。综合利用“地沟油”的一种方法是将“地沟油”中的油脂水解以获取甘油和 。生活中会产生大量废弃塑料,将废弃塑料进行 处理,可以获得乙烯、丙烯等化工原料。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com