
【题目】科学研究发现铂的两种化合物(短线表示化学健)有不同的特性,其中a具有抗癌作用,而b没有;则下列正确的说法是( ) 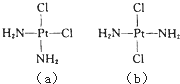
A.a、b分子中,Pt原子与2个Cl原子,2个N原子间形成的结构与CH2Cl2相似
B.a在水中的溶解度比b在水中的溶解度大
C.a、b互为同素异形体
D.a、b是同一物质
 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
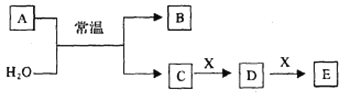
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:___________。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则:
①组成单质A的元素在周期表中的位置为___________。
②A与H2O反应的离子反应方程式为______。
(3)若A为淡黄色粉末,问答下列问题:
①1molA与足量的H2O充分反应时转移的电子数目为________。
②A中所含有的化学键类型为_______。
③若X为一种造成温室效应的气体.则鉴别等浓度的D、E两种溶液,可选择的试剂为____(填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为_________,E是___________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能大量共存的是( )
A.Mg2+、H+、Cl-、HCO3-B.K+、NH4+、NO3-、CO32-
C.NH4+、Na+、SO42-、OH-D.Ag+、Cu2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关氯水的说法正确的是( )
A.能使湿润的有色布条褪色,说明氯水中有Cl2
B.溶液呈黄绿色,有刺激性气味,说明氯水中有Cl2
C.加入盐酸酸化的BaCl2溶液产生白色沉淀,说明氯水中有Cl-
D.加入NaOH溶液,黄绿色消失,说明氯水中有HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图实验装置用于验证某些物质的性质.在试管A中装入足量的固体NaHCO3.试回答下列问题:
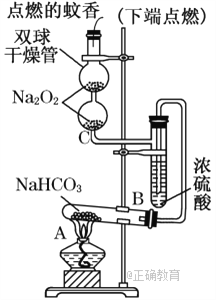
(1)在A试管内发生反应的化学方程式是____________________________________.
(2)B装置的作用是_______________________________________________________.
(3)在双球干燥管内发生反应的化学方程式为___________________________________.
(4)双球干燥管内观察到的实验现象是_________________________________________.上述实验现象说明________________________________________________________.
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是______________________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图各装置进行实验能成功完成相应实验的是
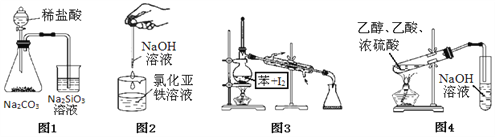
A. 图1:证明非金属性强弱:C>Si B. 图2:制备氢氧化亚铁
C. 图3:分离碘并回收苯 D. 图4:制取和收集乙酸乙酯
【答案】C
【解析】A、稀盐酸易有挥发性,反应产生的二氧化碳中含有氯化氢,能使硅酸钠反应生成硅酸沉淀的不一定是碳酸,故无法证明非金属性C>Si,选项A错误;B、为防止制得的的氢氧化亚铁被氧化,必须将滴管插到液面以下或在液面上加苯覆盖以防止空气中氧气进入溶液氧化产生的氧化亚铁,选项B错误;C、碘溶于苯中,利用沸点的不同蒸馏使苯分离出来并回收苯,实验装置及操作正确,选项C正确;D、制取和收集乙酸乙酯时必须用饱和碳酸钠溶液吸收乙酸乙酯而不能用氢氧化钠溶液,选项D错误。答案选C。
【题型】单选题
【结束】
5
【题目】A、B、C、D、E、F是原子序数依次增大的短周期主族元素。E是同周期元素金属性最强的元素。甲、乙、丙、丁、戊是由上述部分元素中的两种或几种组成的化合物,它们的转化关系如图所示。其中甲是生活中的调味品,丁是淡黄色固体。下列说法不正确的是
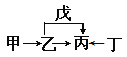
A. 原子半径由大到小的顺序为:r(E)>r(F)>r(C)>r(D)
B. 元素F的氧化物的水物化的酸性一定比硫酸酸性强
C. 元素B的氢化物可能具有正四面体结构
D. 化合物A4BC2D既可能是共价化合物,也可是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某透明澄清的溶液中可能含有NO3- 、Cl- 、SO42-、CO32-、NH4+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等。为确定该溶液的成分,某学习小组做了如下实验:①取该溶液100mL,加入过量NaOH溶液,加热得到0.02mol气体,同时产生红褐色沉淀; ②将沉淀过滤、洗涤、灼烧,得到1.6 g固体; ③向上述滤液中加入足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。下列说法正确的是
A. 不能确定原溶液中是否含有Al3+和K+
B. 原溶液中含有的离子只有:Cl- 、SO42-、NH4+、Fe3+
C. 原溶液中c(NO3-)=0.2 mol·L-1 c(Fe3+)=0.2 mol·L-1
D. 在原溶液中加入足量的铁粉所得溶液中阳离子所带正电荷数减少
【答案】C
【解析】①取该溶液100mL,加入过量NaOH溶液,加热得到0.02mol气体,说明溶液中含有0.02mol NH4+,同时产生红褐色沉淀为氢氧化铁,说明溶液中含有Fe3+,CO32-与Fe3+会发生双水解而不能大量共存,故溶液中一定不含CO32-;②将沉淀过滤、洗涤、灼烧,得到1.6 g固体为氧化铁,则n[Fe(OH)3]=2n(Fe2O3)=2×![]() =0.02mol; ③向上述滤液中加入足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀,则沉淀为硫酸钡,n(SO42-)=n(BaSO4)=
=0.02mol; ③向上述滤液中加入足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀,则沉淀为硫酸钡,n(SO42-)=n(BaSO4)= ![]() =0.02mol。n(+)=n(NH4+)+3n(Fe3+)=0.02mol+3×0.02mol=0.08mol,n(-)=2 n(SO42-)=2×0.02mol=0.04mol<0.08mol,故溶液中还有其他阴离子,且所含阴离子的物质的量相等,故n(-)=2 n(SO42-)+n(NO3-)+n(Cl-)=2×0.02mol+0.02mol+0.02mol=0.08mol,因此溶液中一定含有NO3- 、Cl-,一定不含Al3+和K+。故A.原溶液中一定不含Al3+和K+,选项A错误;B. 原溶液中含有的离子只有:NO3- 、Cl- 、SO42-、NH4+、Fe3+,选项B错误;C. 原溶液中c(NO3-)=0.2 mol·L-1,c(Fe3+)=0.2 mol·L-1,选项C正确;D. 在原溶液中加入足量的铁粉,发生反应:2Fe3++ Fe = 3Fe2+所得溶液中阳离子所带正电荷数基本不变,选项D错误。答案选C。
=0.02mol。n(+)=n(NH4+)+3n(Fe3+)=0.02mol+3×0.02mol=0.08mol,n(-)=2 n(SO42-)=2×0.02mol=0.04mol<0.08mol,故溶液中还有其他阴离子,且所含阴离子的物质的量相等,故n(-)=2 n(SO42-)+n(NO3-)+n(Cl-)=2×0.02mol+0.02mol+0.02mol=0.08mol,因此溶液中一定含有NO3- 、Cl-,一定不含Al3+和K+。故A.原溶液中一定不含Al3+和K+,选项A错误;B. 原溶液中含有的离子只有:NO3- 、Cl- 、SO42-、NH4+、Fe3+,选项B错误;C. 原溶液中c(NO3-)=0.2 mol·L-1,c(Fe3+)=0.2 mol·L-1,选项C正确;D. 在原溶液中加入足量的铁粉,发生反应:2Fe3++ Fe = 3Fe2+所得溶液中阳离子所带正电荷数基本不变,选项D错误。答案选C。
【题型】单选题
【结束】
8
【题目】根据要求回答下列问题:
(1)已知恒温、恒容条件下发生反应:2NO2(g)+2C(s) ![]() N2(g)+2CO2(g)。
N2(g)+2CO2(g)。
①下列图像说明该反应进行到t1时刻未达平衡状态的是________(填选项字母)。
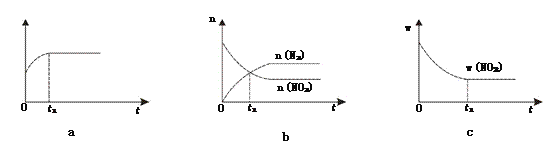
②1 molNO2和足量C发生反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示。
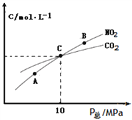
图中A、B、C三点NO2的转化率最高的是_____,该反应的平衡常数Kp=_______(Kp是用平衡分压代替平衡浓度的常数,分压=总压×物质的量分数)。
(2)已知:弱电解质的电离平衡常数为
物质 | H2CO | H2S | HNO2 |
电离平衡常数 (25℃) | Ka1=4.2×10-7 Ka2=5.61×10-11 | Ka1=1.3×10-7 Ka2=7.1×10-15 | Ka=5.1×10-4 |
①含有1L 2mol·L-1碳酸钠的溶液中加入1L 1mol·L-1的HNO2后,则溶液中CO32-、HCO3-和NO2-的离子浓度由大到小是_______。
②25℃时,在0.10 mol·L-1H2S溶液中,通人HCl气体或加入NaOH固体,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。pH=13时,溶液中的c(H2S)+c(HS-)=____mol·L-1;
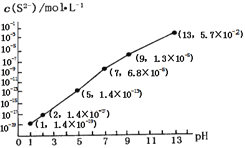
③向10.00mL0.10 mol·L-1的氢硫酸中滴加10.00mL0.1 mol·L-1NaOH溶液,溶液呈_____性,其定量依据是______________________ .
(3)已知:①CaSO4(s)+CO(g)![]() CaO(s)+SO2(g)+CO2(g)△H = +210.5kJmol-1
CaO(s)+SO2(g)+CO2(g)△H = +210.5kJmol-1
②CaSO4(s)+4CO(g)![]() CaS(s)+4CO2(g) △H= -189.2kJmol-1
CaS(s)+4CO2(g) △H= -189.2kJmol-1
则:CaO(s)+3CO(g)+SO2(g) ![]() CaS(s)+3CO2(g) △H=_______kJmol-1.
CaS(s)+3CO2(g) △H=_______kJmol-1.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修3:物质结构与性质】铜、硼、硅、砷等元素的化合物是制造新型激光武器和新型太阳能电池的重要材料。回答下列问题:
(1)基态硅(2814Si)原子中,电子占据的最高能层的轨道数有______个。
(2)已知:蓝色晶体(CuSO4·5H2O)![]() 天蓝色溶液
天蓝色溶液![]() 深蓝色溶液
深蓝色溶液![]() 深蓝色晶体
深蓝色晶体
①蓝色晶体中阴离子的空间构型是_________;
②天蓝色溶液中的阳离子是_____,其配体中心原子的杂化轨道类型是________;
③24.6g深蓝色晶体(其摩尔质量为246g.mol-1)中配离子含有的σ键数是_____;
④实验测得无水乙醇易溶于水,其原因是______________。
(3)砷化镓是具有空间网状结构的晶体,熔点为1230℃,是优良的第三代半导体材料。
①砷化镓属于________晶体。已知氮化硼与砷化镓属于同种晶体类型。则两种晶体熔点较高的是_____(填化学式),其理由是_________。上述两种晶体中的四种元素电负性最小的是_______(填元素符号)。
②砷化镓晶胞结构如图所示。其晶胞边长为a pm,密度为_______g.cm-3。(砷化镓的摩尔质量为M g.mol-1,阿伏伽德罗常数为NA)
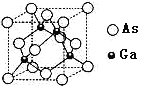
【答案】 9 四面体 [Cu(H2O)4]2+ sp3 1.6NA 乙醇分子与水分子间存在氢键,乙醇分子和水分子都是极性分子 原子晶体 BN 二者均为原子晶体,B、N间的键长比Ga、As的键长短,键能大 Ga 4Mx1030/a3NA
【解析】(1)基态硅(2814Si)原子核外电子数为14,基态原子核外电子排布为1s22s22p63s23p2,电子占据的最高能层符号为M,该能层具有的原子轨道数为1+3+5=9;(2)①蓝色晶体CuSO4·5H2O中阴离子SO42-,根据价层电子对互斥理论,价层电子对个数=σ键+孤电子对个数,SO42-中中心原子S的价层电子对为![]() =4,孤电子对数为
=4,孤电子对数为![]() =0,不含孤电子对,所以空间构型是正四面体结构;②蓝色晶体溶于水得到天蓝色溶液中的阳离子是[Cu(H2O)4]2+;其配体H2O中心原子O原子杂化轨道数为
=0,不含孤电子对,所以空间构型是正四面体结构;②蓝色晶体溶于水得到天蓝色溶液中的阳离子是[Cu(H2O)4]2+;其配体H2O中心原子O原子杂化轨道数为![]() =4,,采取sp3杂化方式;③每个配离子[Cu(NH3)4]2+含有的σ键数是3×4+4=16,故24.6g深蓝色晶体{[Cu(NH3)4]SO4H2O }为0.1mol,其中配离子[Cu(NH3)4]2+含有的σ键数是0.1mol×16×NA mol-1=1.6NA;④乙醇分子与水分子间存在氢键,乙醇分子和水分子都是极性分子,故无水乙醇易溶于水;(3)①砷化镓是具有空间网状结构的晶体,熔点为1230℃,是优良的第三代半导体材料,与晶体硅相似,故砷化镓属于原子晶体;氮化硼与砷化镓都属于原子晶体,B、N间的键长比Ga、As的键长短,键能大,故BN晶体熔点较高;非金属性越强,电负性越强,则B、N、Ga、As四种元素电负性最小的Ga;②一个晶胞中含有As 8×
=4,,采取sp3杂化方式;③每个配离子[Cu(NH3)4]2+含有的σ键数是3×4+4=16,故24.6g深蓝色晶体{[Cu(NH3)4]SO4H2O }为0.1mol,其中配离子[Cu(NH3)4]2+含有的σ键数是0.1mol×16×NA mol-1=1.6NA;④乙醇分子与水分子间存在氢键,乙醇分子和水分子都是极性分子,故无水乙醇易溶于水;(3)①砷化镓是具有空间网状结构的晶体,熔点为1230℃,是优良的第三代半导体材料,与晶体硅相似,故砷化镓属于原子晶体;氮化硼与砷化镓都属于原子晶体,B、N间的键长比Ga、As的键长短,键能大,故BN晶体熔点较高;非金属性越强,电负性越强,则B、N、Ga、As四种元素电负性最小的Ga;②一个晶胞中含有As 8×![]() +6×
+6×![]() =4个,Ga在内部,共4个,即一个晶胞中含有4个砷化镓,其晶胞边长为apm=a×10-10cm,V=a3×10-30cm3,密度为
=4个,Ga在内部,共4个,即一个晶胞中含有4个砷化镓,其晶胞边长为apm=a×10-10cm,V=a3×10-30cm3,密度为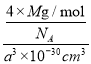 =
=![]() 。
。
点睛:本题考查了方程式的书写、分子空间构型以及杂化类型的判断、晶胞密度计算等知识,题目难度较大,注意相关基础的把握和方法的积累。先根据分摊法计算每个晶胞含有多少个原子,再根据晶胞的边长,确定晶胞的体积,再根据ρ=![]() 计算密度。
计算密度。
【题型】综合题
【结束】
12
【题目】【化学—选修5:有机化学基础】PVB是重要的建筑材料。其合成路线如下(部分反应条件和产物略去)。
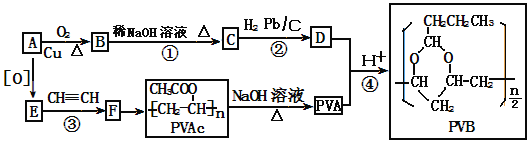
已知:
Ⅰ.A分子式为C2H6O,其核磁共振氢谱图显示有三个波峰。
![]()
Ⅲ. ![]()
回答下列问题:
(1)A的结构简式_______,B→C的反应类型有加成反应和_______,D的官能团为_______。
(2)PVAC的名称是___________(3)C分子中最多有_____个原子共平面。
(3)E→F的反应方程式为_____________。
(4)已知-OH直接连在不饱和C原子上不稳定,会自动发生分子内重排形成-CHO。则D的同分异构体中能与金属Na反应产生H2的有____种。
(5)以溴乙烷为原料制备丁醛(其他无机试剂任选),其流程图为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。
锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s),
下列说法错误的是( )
A. 电池工作时,锌失去电子
B. 电池工作时,电子由负极通过外电路流向正极
C. 电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e-=Mn2O3(s)+2OH-(aq)
D. 外电路中每通过0.4mol电子,锌的质量理论上减小6.5g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com