
取NaOH溶液50mL,通入一定量CO2,再向溶液中逐滴加入0.1mol/L盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列说法错误的是
| A.原NaOH溶液中通入CO2后,所得溶液中c(CO32-)小于C(HCO3-) |
| B.NaOH溶液中,Na+的物质的量浓度为0.18 mol/L |
| C.NaOH溶液中通入CO2后,再加入足量盐酸产生CO2气体体积(标准状况)1344mL。 |
| D.0—30mL之间的离子方程式:CO32-+H+→HCO3- |
A
解析考点:离子方程式的有关计算;离子浓度大小的比较.
分析:由图可知,0~30mL没有气体生成,从30mL开始加盐酸生成二氧化碳气体,共消耗盐酸90mL-30mL=60mL,则NaOH溶液50mL,通入一定量CO2反应后溶液中的溶质为Na2CO3、NaHCO3,且二者的量相同,然后利用盐酸的物质的量来计算Na+的物质的量浓度及二氧化碳气体的体积.
解:因0~30mL没有气体生成,从30mL开始加盐酸生成二氧化碳气体,共消耗盐酸90mL-30mL=60mL,两个过程消耗的酸的体积比为1:2,
则NaOH溶液通入一定量CO2反应后溶液中的溶质为等物质的量的Na2CO3、NaHCO3,
A、等物质的量的Na2CO3、NaHCO3,则所得溶液中c(CO32-)=c(HCO3-),故A错误;
B、由HCl~NaCl~NaOH,则NaOH的物质的量为0.09L×0.1mol/L=0.009mol,Na+的物质的量浓度为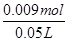 =0.18mol/L,故B正确;
=0.18mol/L,故B正确;
C、等物质的量的Na2CO3、NaHCO3,其物质的量为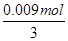 =0.003mol,由碳原子守恒可知二氧化碳的物质的量为0.003mol×2=0.006mol,则加入足量盐酸产生CO2气体体积在标准状况下为0.006mol×22.4L/mol=1344mL,故C正确;
=0.003mol,由碳原子守恒可知二氧化碳的物质的量为0.003mol×2=0.006mol,则加入足量盐酸产生CO2气体体积在标准状况下为0.006mol×22.4L/mol=1344mL,故C正确;
D、0~30mL,发生碳酸钠与盐酸反应生成碳酸氢钠和氯化钠,其离子方程式为CO32-+H+═HCO3-,故D正确;
故选A.


科目:高中化学 来源: 题型:阅读理解
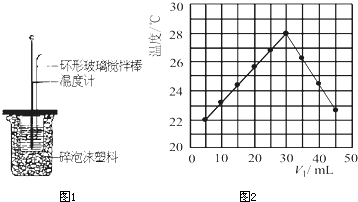
| 温度 | 起始温度t1/℃ | 终止温度 t1/℃ |
温度差 (t2-t1)t1/℃ | ||
| 实验次数 | H2SO4 | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 4.0 4.0 |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
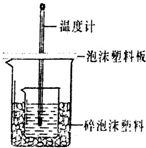 某实验小组设计用0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行测定中和热的实验.
某实验小组设计用0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行测定中和热的实验.| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 温差(t2-t1)℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.3 | 3.3 |
| 2 | 25.1 | 25.1 | 25.1 | 28.5 | 3.4 |
| 3 | 25.1 | 25.1 | 25.1 | 28.6 | 3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
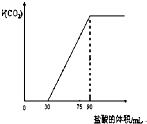 取NaOH溶液50mL,通入一定量CO2,再向溶液中逐滴加入0.1mol/L盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列说法错误的是( )
取NaOH溶液50mL,通入一定量CO2,再向溶液中逐滴加入0.1mol/L盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列说法错误的是( )| A、原NaOH溶液中通入CO2后,所得溶液中c(CO32-)小于c(HCO3-) | B、NaOH溶液中,Na+的物质的量浓度为0.18mol/L | C、NaOH溶液中通入CO2后,再加入足量盐酸产生CO2气体体积(标准状况)1344mL | D、0-30mL之间的离子方程式:CO32-+H+═HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
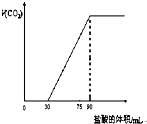 取NaOH溶液50mL,通入一定量CO2,再向溶液中逐滴加入0.1mol/L盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列说法错误的是
取NaOH溶液50mL,通入一定量CO2,再向溶液中逐滴加入0.1mol/L盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列说法错误的是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com