
20℃时饱和KCl溶液的密度为1.174 g·cm-3,物质的量浓度为4.0 mol·L-1,则下列说法中不正确的是( )
A、25℃时,饱和KCl溶液的浓度大于4.0 mol·L-1
B此溶液中KCl的质量分数为 ×100%
×100%
C20℃,密度小于1.174 g·cm-3的KCl溶液是不饱和溶液
D将此溶液蒸发部分水再恢复到20℃时,溶液密度一定大于1.174 g·cm-3
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
把0.05molNaOH固体分别加入到下列100ml液体中,溶液的导电性基本不变,该液体是( )
A. 自来水 B. 0.5mol·盐酸 C. 0.5mol·醋酸 D.0.5mol·氯水
查看答案和解析>>
科目:高中化学 来源: 题型:
分析下表中的四个热化学方程式,判断氢气和丙烷的燃烧热分别是
| “神十” 发射 火箭 燃料 | 液氢 (H2) | ①2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1 ②2H2(l)+O2(l)===2H2O(g) ΔH=-482.6 kJ·mol-1 |
| 奥运会 火炬 燃料 | 丙烷 (C3H8) | ③C3H8(l)+5O2(g)===3CO2(g)+4H2O(g) ΔH=-2 013.8 kJ·mol-1 ④C3H8(g |
A.571.6 kJ·mol-1,2 221.5 kJ·mol-1
B.241.3 kJ·mol-1,2 013.8 kJ·mol-1
C.285.8 kJ·mol-1,2 013.8 kJ·mol-1
D.285.8 kJ·mol-1,2 221.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
能源危机是当前全球性的问题,“开源节流”是应对能源危机的重要举措。
请回答下列问题:
(1)下列做法不利于能源“开源节流”的是________(填序号)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气,以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源,减少煤、石油等化石燃料的使用
d.减少资源消耗,增加资源的重复使用,注重资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧生成二氧化碳,反应放出的热量如图所示:

①在通常状况下,________(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为ΔH=________。
②12 g石墨与24 g氧气反应生成气体,该过程放出的热量为________。
 (3)综合上述有关信息,请写出CO和NO反应的热化学方程式:________________________________________________________________________。
(3)综合上述有关信息,请写出CO和NO反应的热化学方程式:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对电解质概念的理解正确的是( )
A.在水溶液中或熔融状态下能导电的物质
B.凡在水中能生成离子因而能导电的物质
C.氧化钠溶于后水溶液能导电,但溶液中的离子并非本身电离,因而氧化钠是非电解质
D.在水溶液里或熔融状态下本身能电离出阳离子和阴离子,因而是能导电的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
标出下列反应中电子转移的方向和数目并回答问题:
3H2O2 + 2H2CrO4 = 2 Cr(OH)3 + 3O2 + 2H2O
(1)该反应中的还原剂是___________,被还原的元素________,还原产物是__________;
(2)反应转移了0.3mol电子,则产生的气体在标准状态下体积约为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.用金属钠可区分乙醇和乙醚
B.用高锰酸钾酸性溶液可区分己烷和3己烯
C.用水可区分苯和溴苯
D.用新制的银氨溶液可区分甲酸甲酯和乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
美国化学家R.F.Heck因发现如下Heck反应而获得2010年诺贝尔化学奖。
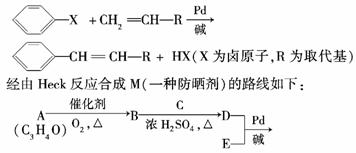
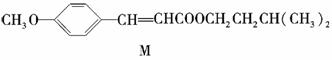
回答下列问题:
(1)M可发生的反应类型是________。
a.取代反应 b.酯化反应
c.缩聚反应 d.加成反应
(2)C与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,F的结构简式是________________________________________________________________________。
D在一定条件下反应生成高分子化合物G,G的结构简式是_____________________。
(3)在A→B的反应中,检验A是否反应完全的试剂是________。
(4)E的一种同分异构体K符合下列条件:苯环上有两个取代基且苯环上只有两种不同 化学环境的氢,与FeCl3溶液作用显紫色。K与过量NaOH溶液共热,发生反应的方程式为___________________________________________________________________。
化学环境的氢,与FeCl3溶液作用显紫色。K与过量NaOH溶液共热,发生反应的方程式为___________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇燃料电池工作原理如下图,下列说法不正确的是
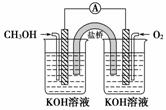
A.盐桥中的K+向负极移动
B.负极电极反应方程式为:
CH3OH-6e-+8OH-===CO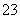 +6H2O
+6H2O
C.每消耗1 mol甲醇,需消耗33.6 L标况下的氧气
D.正极烧杯中溶液pH增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com