
把0.05molNaOH固体分别加入到下列100ml液体中,溶液的导电性基本不变,该液体是( )
A. 自来水 B. 0.5mol·盐酸 C. 0.5mol·醋酸 D.0.5mol·氯水
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
同周期元素W、X、Y、Z的原子序数依次增大,W、X原子的最外电子层电子数之比为4︰3,Z原子比X原子的核外电子数多4。下列说法正确的是
A. W、Y、Z的电负性大小顺序一定是Z>Y>W
B. W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z
C.Y、Z形成的分子的空间构型可能是正四面体
D.WY2分子中σ键与π键的数目之比是2︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
下图装置可以用来制取、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于( )
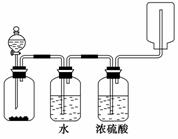
A.锌和盐酸制备氢气
B.二氧化锰与浓盐酸制备氯气
C.碳酸钙和盐酸制备二氧化碳
D.氯化钠和浓硫酸制备氯化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
准确量取25.00 mL酸性高锰酸钾溶液,可选用的仪器是( )
A.500 mL量筒 B.10 mL量筒
C.50 mL酸式滴定管 D.50 mL碱式滴定管
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是元素周期表的一部分,下列说法正确的是( )
A.可在灰色区域“甲”中寻找催化剂
B.离子半径:W-﹥X+﹥Y3-
C.气态氢化物的稳定性:Z﹥W
D.工业上电解X和W化合物的水溶液制备X

查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式正确的是 ( )
A.甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为
CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为
N2(g)+3H2(g)  2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
C.已知在101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为
H2(g)+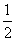 O2(g)===H2O(g) ΔH=-242 kJ·mol-1
O2(g)===H2O(g) ΔH=-242 kJ·mol-1
D.25 ℃,101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ·mol-1,硫酸溶液与氢氧化钾溶液反应的中和热的热化学方程式为
H2SO4(aq)+2KOH(aq)===K2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
20℃时饱和KCl溶液的密度为1.174 g·cm-3,物质的量浓度为4.0 mol·L-1,则下列说法中不正确的是( )
A、25℃时,饱和KCl溶液的浓度大于4.0 mol·L-1
B此溶液中KCl的质量分数为 ×100%
×100%
C20℃,密度小于1.174 g·cm-3的KCl溶液是不饱和溶液
D将此溶液蒸发部分水再恢复到20℃时,溶液密度一定大于1.174 g·cm-3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com