
下列变化需克服相同类型作用力的是
A.碘和干冰的升华 B.硅和C60的熔化
C.氯化氢和氯化钾的溶解 D.溴和汞的气化
科目:高中化学 来源: 题型:
4种相邻主族短周期元素的相对位置如表,元素X的原子核外电子数是M的2倍,Y的氧化物具有两性。回答下列问题:
| M | N | ||
| X | Y |
(1)元素X在周期表中的位置是第________周期、第________族,其单质可采用电解熔融________的方法制备。
(2)M、N、Y三种元素最高价氧化物对应的水化物中,酸性最强的是________,碱性最强的是________。(填化学式)
(3)气体分子(MN)2的电子式为________。(MN)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
把0.05molNaOH固体分别加入到下列100ml液体中,溶液的导电性基本不变,该液体是( )
A. 自来水 B. 0.5mol·盐酸 C. 0.5mol·醋酸 D.0.5mol·氯水
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中一定能大量共存的是( )
A.pH=0的溶液中:ClO-、Cu2+、SO 、K+
、K+
B.使pH试纸变红色的溶液中:Fe2+、I-、NO3-、Cl-
C.能够和金属镁反应放出气体的溶液中:Na+、H+、SO 、Cl-
、Cl-
D.常温下,水电离出的c(H+)与c(OH-)乘积为10-28的溶液中:K+、Na+、HS-、Ca2+
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组为了探究“铁与水蒸气”的反应的产物,进行了下列实验:用如图所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒高温下不与水和铁反应).
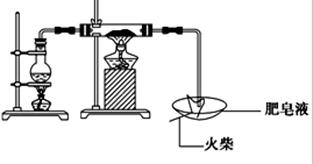
(1)如何检查该装置的气密性:
(2)写出铁与水蒸气反应的化学方程式
(3)验证固体产物中铁元素的价态
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;1mol/L CuSO4、3mol/L H2SO4、3mol/L HNO3、30%H2O2、0.01mol/L KMnO4、20%KSCN、蒸馏水。
在答题卡上按下表的格式写出实验步骤、预期现象与结论。
| 实验步骤 | 预期现象与结论 | |
| 步骤1 | 取反应后干燥的固体ag于试管中,加入足量的1mol/L CuSO4溶液,充分振荡,经固液分离、洗涤后,再向固体中滴加足量的 ,振荡溶解,过滤后将滤液配成250mL溶液,待用。 | |
| 步骤2 | 取少量步骤1中滤液于试管中,
|
|
| 步骤3 | 取少量步骤1中滤液于试管中,
|
|
步骤1中加入足量1mol/L CuSO4溶液的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
硅是重要的半导体材料,构成了现代电子工业的基础。回答下列问题:
(1)硅主要以硅酸盐、____________等化合物的形式存在于地壳中。
(2)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以________相结合,其晶胞中共有8个原子,其中在面心位置贡献________个原子。
(3)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为______________________________________。
(4)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C—C | C—H | C—O | Si—Si | Si—H | Si—O |
| 键能/ (kJ·mol-1) | 356 | 413 | 336 | 226 | 318 | 452 |
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是________________________________________________________________________。
②SiH4的稳定性小于CH4,更易生成氧化物,原因是________________________________
________________________________________________________________________。
(5)在硅酸盐中,SiO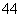 四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为__________,Si与O的原子数之比为__________,化学式为__________。
四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为__________,Si与O的原子数之比为__________,化学式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
分析下表中的四个热化学方程式,判断氢气和丙烷的燃烧热分别是
| “神十” 发射 火箭 燃料 | 液氢 (H2) | ①2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1 ②2H2(l)+O2(l)===2H2O(g) ΔH=-482.6 kJ·mol-1 |
| 奥运会 火炬 燃料 | 丙烷 (C3H8) | ③C3H8(l)+5O2(g)===3CO2(g)+4H2O(g) ΔH=-2 013.8 kJ·mol-1 ④C3H8(g |
A.571.6 kJ·mol-1,2 221.5 kJ·mol-1
B.241.3 kJ·mol-1,2 013.8 kJ·mol-1
C.285.8 kJ·mol-1,2 013.8 kJ·mol-1
D.285.8 kJ·mol-1,2 221.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
能源危机是当前全球性的问题,“开源节流”是应对能源危机的重要举措。
请回答下列问题:
(1)下列做法不利于能源“开源节流”的是________(填序号)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气,以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源,减少煤、石油等化石燃料的使用
d.减少资源消耗,增加资源的重复使用,注重资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧生成二氧化碳,反应放出的热量如图所示:

①在通常状况下,________(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为ΔH=________。
②12 g石墨与24 g氧气反应生成气体,该过程放出的热量为________。
 (3)综合上述有关信息,请写出CO和NO反应的热化学方程式:________________________________________________________________________。
(3)综合上述有关信息,请写出CO和NO反应的热化学方程式:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
美国化学家R.F.Heck因发现如下Heck反应而获得2010年诺贝尔化学奖。
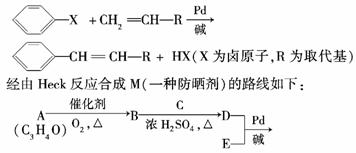
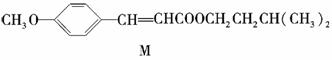
回答下列问题:
(1)M可发生的反应类型是________。
a.取代反应 b.酯化反应
c.缩聚反应 d.加成反应
(2)C与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,F的结构简式是________________________________________________________________________。
D在一定条件下反应生成高分子化合物G,G的结构简式是_____________________。
(3)在A→B的反应中,检验A是否反应完全的试剂是________。
(4)E的一种同分异构体K符合下列条件:苯环上有两个取代基且苯环上只有两种不同 化学环境的氢,与FeCl3溶液作用显紫色。K与过量NaOH溶液共热,发生反应的方程式为___________________________________________________________________。
化学环境的氢,与FeCl3溶液作用显紫色。K与过量NaOH溶液共热,发生反应的方程式为___________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com