
下图装置可以用来制取、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于( )
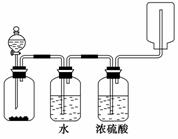
A.锌和盐酸制备氢气
B.二氧化锰与浓盐酸制备氯气
C.碳酸钙和盐酸制备二氧化碳
D.氯化钠和浓硫酸制备氯化氢
科目:高中化学 来源: 题型:
下列说法中正确的是
A.两个原子或多个原子之间的相互作用叫做共价键
B.阴、阳离子间通过静电引力而形成的化学键叫做离子键
C.只有金属元素和非金属元素化合时才能形成离子键
D.大多数的盐、碱和低价金属氧化物中含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
4种相邻主族短周期元素的相对位置如表,元素X的原子核外电子数是M的2倍,Y的氧化物具有两性。回答下列问题:
| M | N | ||
| X | Y |
(1)元素X在周期表中的位置是第________周期、第________族,其单质可采用电解熔融________的方法制备。
(2)M、N、Y三种元素最高价氧化物对应的水化物中,酸性最强的是________,碱性最强的是________。(填化学式)
(3)气体分子(MN)2的电子式为________。(MN)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列排序正确的是( )
A.酸性:H2CO3<C6H5OH<H3COOH
B.碱性:Ba(OH)2<Ca(OH)2<KOH
C.熔点:MgBr2<SiCl4<BN
D.沸点:PH3<NH3<H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1) 五种元素原子半径由大到小的顺序是(写元素符号)————————
(2) X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式)————
(3) 由以上某些元素组成的化合物A、B、C、D有如下转化关系
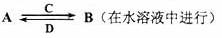
其中C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式——;D的电子式——
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为——
由A转化为B的离子方程式——————
②如果A由三种元素组成 ,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因——————————————————。A、B浓度均为0.1mol/L的混合溶液中,离子浓度由大到小的顺序是——————————;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有————————————。
,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因——————————————————。A、B浓度均为0.1mol/L的混合溶液中,离子浓度由大到小的顺序是——————————;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有————————————。
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸亚铁铵
[(NH4)2SO4·FeSO4·6H2O]为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1 将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2 向处理过的铁屑中加入过量的3 mol·L-1 H2SO4溶液,在60 ℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液。
步骤3 向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)在步骤1的操作中,下列仪器中不必用到的有________(填仪器编号);
①铁架台 ②燃烧匙 ③锥形瓶 ④广口瓶 ⑤研钵
⑥玻璃棒 ⑦酒精灯
(2)在步骤2中所加的硫酸必须过量,其原因是________________________________________________;
(3)在步骤3中,“一系列操作”依次为____________、__________和过滤;
(4) 本实验制的硫酸亚铁铵晶体常含有Fe3+杂质。检验Fe3+常用的试剂是____________,可以观察到的现象是_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
把0.05molNaOH固体分别加入到下列100ml液体中,溶液的导电性基本不变,该液体是( )
A. 自来水 B. 0.5mol·盐酸 C. 0.5mol·醋酸 D.0.5mol·氯水
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中一定能大量共存的是( )
A.pH=0的溶液中:ClO-、Cu2+、SO 、K+
、K+
B.使pH试纸变红色的溶液中:Fe2+、I-、NO3-、Cl-
C.能够和金属镁反应放出气体的溶液中:Na+、H+、SO 、Cl-
、Cl-
D.常温下,水电离出的c(H+)与c(OH-)乘积为10-28的溶液中:K+、Na+、HS-、Ca2+
查看答案和解析>>
科目:高中化学 来源: 题型:
能源危机是当前全球性的问题,“开源节流”是应对能源危机的重要举措。
请回答下列问题:
(1)下列做法不利于能源“开源节流”的是________(填序号)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气,以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源,减少煤、石油等化石燃料的使用
d.减少资源消耗,增加资源的重复使用,注重资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧生成二氧化碳,反应放出的热量如图所示:

①在通常状况下,________(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为ΔH=________。
②12 g石墨与24 g氧气反应生成气体,该过程放出的热量为________。
 (3)综合上述有关信息,请写出CO和NO反应的热化学方程式:________________________________________________________________________。
(3)综合上述有关信息,请写出CO和NO反应的热化学方程式:________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com