
硫酸亚铁铵
[(NH4)2SO4·FeSO4·6H2O]为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1 将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2 向处理过的铁屑中加入过量的3 mol·L-1 H2SO4溶液,在60 ℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液。
步骤3 向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)在步骤1的操作中,下列仪器中不必用到的有________(填仪器编号);
①铁架台 ②燃烧匙 ③锥形瓶 ④广口瓶 ⑤研钵
⑥玻璃棒 ⑦酒精灯
(2)在步骤2中所加的硫酸必须过量,其原因是________________________________________________;
(3)在步骤3中,“一系列操作”依次为____________、__________和过滤;
(4) 本实验制的硫酸亚铁铵晶体常含有Fe3+杂质。检验Fe3+常用的试剂是____________,可以观察到的现象是_________________________________________________。
科目:高中化学 来源: 题型:
PH3一种无色剧毒气体,其分子结构和NH3相似,但P—H键键能比N—H键键能低。下列判断错误的是
A.PH3分子呈三角锥形
B.PH3分子是极性分子
C.PH3沸点低于NH3沸点,因为P-H键键能低
D.PH3分子稳定性低于NH3分子,因为N—H键键能高
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是________,写出一种工业制备单质F的离子方程式:__________________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为__________,其水溶液与F单质反应的化学方程式为____________________________________________;在产物中加入少量KI,反应后加入CCl4并振荡,有机层显______色。
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1∶1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为________;b的化学式为______________;c的电子式为________;d的晶体类型是________。
(4)由A和B、D元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过________键构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
四种短周期元素在周期表中的位置如右图,其中只有M为金属元素。下列说法不正确的是
A.原子半径Z<M
B.Y的最离价氧化物对应水化物的酸性比X 的弱
C.X 的最简单气态氢化物的热稳 定性比Z的小
定性比Z的小
D.Z位于元索周期表中第2 周期、第ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
下图装置可以用来制取、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于( )
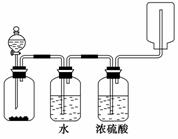
A.锌和盐酸制备氢气
B.二氧化锰与浓盐酸制备氯气
C.碳酸钙和盐酸制备二氧化碳
D.氯化钠和浓硫酸制备氯化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关滴定操作的顺序正确的是( )
①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液
③检查滴定管是否漏水 ④滴定 ⑤洗涤
A.⑤①②③④ B.③⑤①②④ C.③①⑤②④ D.⑤①③②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是元素周期表的一部分,下列说法正确的是( )
A.可在灰色区域“甲”中寻找催化剂
B.离子半径:W-﹥X+﹥Y3-
C.气态氢化物的稳定性:Z﹥W
D.工业上电解X和W化合物的水溶液制备X

查看答案和解析>>
科目:高中化学 来源: 题型:
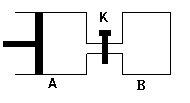
如图所示,容器A左侧是可平行移动的活塞。向A中充入1molX和1molY,向B中充入2molX和2molY,起始时V(A)=V(B)=aL。在相同温度和有催化剂存在的条件下,两容器各自发生:X(g)+Y(g)  Z(g)+2W(g),
Z(g)+2W(g),
达到平衡时V(A)=1.2aL。试回答:
⑴A中X的转化率为 。
⑵A、B中X转化率大小关系为A B(填“>”、“<”、“=” )
⑶打开K,一段时间后又达到新的平衡时,A的体积为 L(连通管中气体体积不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿弗加德罗常数,下列说法正确的是
A.0.2 mol H2O2完全分解转移的电子数为0.4NA
B.300 mL 2 mol·L-1的蔗糖溶液中所含分子数为0.6NA
C.在标准状况下,2.8g N2和2.8g CO所含电子数均为1.4NA
D.在常温常压下,2.24L SO2与O2混合气体中所含氧原子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com