
已知NO2和N2O4可以相互转化: N2O4 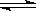 2NO2,某温度时,把1mol N2O4气体通入体积为10L的真空密闭容器中,立即出现棕色,反应进行4s时NO2的浓度为0.04mol/L,再经过一定时间后,反应到达平衡,这时容器内压强为开始时的1.8倍。
2NO2,某温度时,把1mol N2O4气体通入体积为10L的真空密闭容器中,立即出现棕色,反应进行4s时NO2的浓度为0.04mol/L,再经过一定时间后,反应到达平衡,这时容器内压强为开始时的1.8倍。
(1)前4s中以N2O4的浓度变化表示的平均反应速度为 mol/L·s
(2)在4s时容器内的压强为开始时的 倍
(3)在平衡时容器内含N2O4 mol
(4)在平衡时容器内NO2的浓度为 mol/L
(5)平衡时N2O4的转化率为
(1)0.005mol/(L·s)(2)1.2倍(3)0.2mol(4)0.16mol/L (5)80%
解析试题分析:N2O4 2 NO2
2 NO2
(1)反应进行4s时NO2的浓度为0.04mol/L;则v(NO2)="0.04mol/L" / 4s="0.04mol/(L·s)" ;v(N2O4)/v(NO2)=1/2,故前4秒以N2O4浓度变化表示的平均反应速率为0.005mol/(L·s)
(2)等温等容,压强与气体的物质的量成正比。则4秒时,n(NO2)="0.04mol/L" * 10L = 0.4mol
参加反应的N2O4为0.2mol,则此时容器内气体总物质的量为1mol-0.2mol+0.4mol=1.2mol,起始是容器中只有1mol N2O4气体,则在4s时容器内的压强为开始时的1.2倍;
(3)平衡时压强为开始的1.8倍,则平衡时容器内气体物质的量为1.8mol,设参加反应的N2O4为x,则有(1-x)+2x=1.8 解得:x=0.8mol,则在平衡时容器内含N2O4 的物质的量为:1mol-0.8mol=0.2mol;
(4)由于在平衡时容器内含N2O4 0.8mol,故此时容器内NO2的浓度为(0.8*2)/10 mol/L =0.16mol/L,则在平衡时容器内NO2的浓度为0.16mol/L;
(5)平衡时消耗的N2O4物质的量为:0.8mol ,则平衡时N2O4的转化率为:0.8mol/1mol=80% ;
考点:可逆反应、化学反应速率、转化率
点评:化学反应速率为高考重要考点之一,基础演算能力的要求较高,而且全面要求考生对可逆反应、化学反应速率等相关知识的理解与熟练掌握,具有一定的分析力度与考查难度,考生平时应当多注重化学反应速率相关内容的实践练习。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图所示.
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图所示.| 10 |
| 9 |
| 10 |
| 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
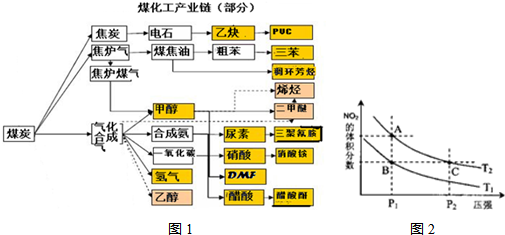
| c(H2)c(CO) |
| c(H2O) |
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
 和
和 .实验测得N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式
.实验测得N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:
 (2009?宿迁二模)已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )
(2009?宿迁二模)已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)(正反应为放热反应).现将一定量NO2 和N2O4 的混合气体通入一体积为1L的恒温密闭容器中,反应物的浓度随时间变化的关系曲线如图所示.请回答下列问题:
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)(正反应为放热反应).现将一定量NO2 和N2O4 的混合气体通入一体积为1L的恒温密闭容器中,反应物的浓度随时间变化的关系曲线如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
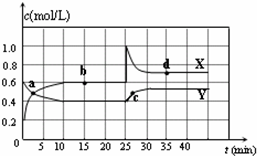 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )| A、图中的两条曲线,X是表示NO2浓度随时间的变化曲线 | B、a、b、c、d四个点中,只有b、d点的化学反应处于平衡状态 | C、25 min时,导致平衡移动的原因是将密闭容器的体积缩小为1L | D、前10 min内用v(NO2)表示的化学反应速率为0.06 mol/(L?min) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com