
����Ŀ�������ֽ�������A��B��C������A����ɫ��ӦΪ��ɫ��B��C�dz������������ֽ�������A��B��C��������ס��ҡ���������D��E��F��G��H֮�䷢������ת����ϵ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ���������
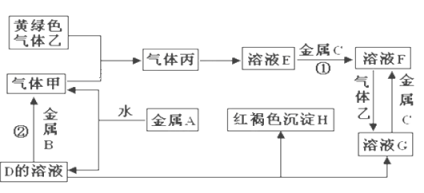
�����������Ϣ�ش��������⣺
��1��д���������ʵĻ�ѧʽ��A__________��H______��G_______����_______��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ
��Ӧ��_____________________________________________________
��Ӧ��_____________________________________________________
��3��F��Һ�������ҷ�Ӧ�����ӷ���ʽ______________________________
���𰸡�Na Fe(OH)3 FeCl3 Cl2 Fe+2HCl=FeCl2+H2�� 2Al+2NaOH+2H2O=2NaAlO2+3H2�� 2Fe2++Cl2=2Fe3++2Cl-
��������
A�ǽ������ʣ�������ɫ��ӦΪ��ɫ����A��Na������ɫ��������Cl2�����ɫ������H��Fe��OH��3��Na��ˮ��Ӧ����NaOH��H2�������H2��D��NaOH������B�ܺ�NaOH��Һ��Ӧ������������B��Al��������������Ӧ����HCl�������HCl��E�����ᣬ�����C��Ӧ����F��F�ܺ�������Ӧ����G��G��NaOH��Ӧ����Fe��OH��3����G��FeCl3��F��FeCl2��C��Fe���ٽ����Ŀ�������
��1��ͨ�����Ϸ���֪��A��Na��H��Fe��OH��3��G��FeCl3������Cl2��
�ʴ�Ϊ��Na��Fe(OH)3��FeCl3��Cl2��
��2����Ӧ����Fe������ķ�Ӧ�����仯ѧ����ʽΪ��Fe+2HCl=FeCl2+H2����
��Ӧ��Ϊ����Al��NaOH��Һ��Ӧ����ƫ�����ƺ������Ĺ��̣����仯ѧ����ʽΪ��2Al+2NaOH+2H2O=2NaAlO2+3H2����
�ʴ�Ϊ��Fe+2HCl=FeCl2+H2����2Al+2NaOH+2H2O=2NaAlO2+3H2����
��3��F��ҺΪFeCl2��������ΪCl2�������߷�Ӧ�����ӷ���ʽΪ��2Fe2++Cl2=2Fe3++2Cl-��
�ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����
A. ��״���£�11.2LNO��11.2LO2��Ϻ�����ķ�������ΪNA
B. ��״���£���H2O2�Ƶ�4.48LO2ת�Ƶĵ�����ĿΪ0.8NA
C. 14g����ϩ�뻷������ɵĻ�����庬�е�̼ԭ����ĿΪNA
D. 25��ʱ��pH =13��Ba(OH)2��Һ�к���OH������ĿΪ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ϣ�����Ĺؼ����ϣ��ڹ�ҵ�п�����þ��ȡ��:2Mg(����)+SiO2![]() 2MgO+Si��2Mg+Si
2MgO+Si��2Mg+Si![]() Mg2Si(����Ӧ)�������ϵ�:��Mg2Si������Ѹ�ٷ�Ӧ����SiH4(����)����SiH4�ڳ�������һ�ֲ��ȶ��ֽ⡢����ȼ�����壻��Mg�ڼ���ʱ����CO2��N2��Ӧ��
Mg2Si(����Ӧ)�������ϵ�:��Mg2Si������Ѹ�ٷ�Ӧ����SiH4(����)����SiH4�ڳ�������һ�ֲ��ȶ��ֽ⡢����ȼ�����壻��Mg�ڼ���ʱ����CO2��N2��Ӧ��
I.��ͼ��ʵ���ҽ���Mg��SiO2��Ӧ���b��:
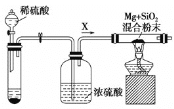
(1)ʢ��ϡ�����װ��Ϊ_________________�����������Ĵ��ڶԸ�ʵ���нϴ�Ӱ�죬ʵ����Ӧͨ������X��Ϊ���������Թ��еĹ���ҩƷ��ѡ��_________(�����)��
a.ʯ��ʯ b.п�� c.����
(2)��Ӧ��������ȴ������ʱ������Ӧ��Ļ�����м���ϡ���ᡣ�ɹ۲쵽�����Ļ��ǣ������������ԭ���û�ѧ����ʽ��ʾΪ ��____________________�� ��_________________��
II.������ͼװ��(�����ܡ�0���̶��ڿ̶��ߵ����Ϸ�)�ɲⶨ������Ĵ��ȡ�
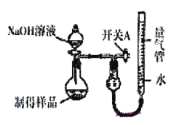
(3)ʵ�鿪ʼǰӦ��_________________��
(4)��ȡ��ƷWg����5mLNaOH(����)��ַ�Ӧ����Ӧǰ������Һ�����ΪV1mL����Ӧ��ΪV2mL(ʵ�����ݾ�ת��Ϊ��״����)������Ʒ�Ĵ���Ϊ____________________����д������ʽ��������
(5)����Ӧ����ʱ����ǰδ��������װ������Һ��߶���ƽ(�ұߵ�Һ��������Һ��)����ᵼ��ʵ����______(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NO2װ����л������ܱ������У�����Ӧ2NO2(g)![]() N2O4(g)�ﵽƽ��ı�����һ������������������ȷ����
N2O4(g)�ﵽƽ��ı�����һ������������������ȷ����
A. �����¶ȣ�������ɫ�����˷�ӦΪ���ȷ�Ӧ
B. ����ѹ�����������ƽ��������Ӧ�����ƶ�������������ɫ��dz
C. ����ѹ������������������Сһ�룬ѹǿ����С��ԭ��������
D. ���º���ʱ������ϡ�����壬ѹǿ����ƽ��������Ӧ�����ƶ�������������ɫ��dz
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������HCl��AlCl3�Ļ����Һ�м���NaOH��Һ�����ɵij����ͼ���NaOH��Һ�������ϵ�Ĵ���ͼ��Ϊ
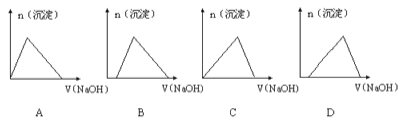
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������AlCl3��MgCl2�����Һ������һ����������������NaOH��Һ�����ɳ��������ʵ��������NaOH�����ʵ����Ĺ�ϵ��ͼ��ʾ����:
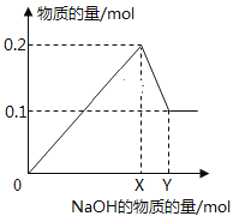
��1��O-X�η�Ӧ�����ӷ���ʽΪ��________________________��
��2��X-Y�η�Ӧ�����ӷ���ʽΪ_________________________
��3������Mg(OH)2������Ϊ___________________g��
��4��X=________________��Y=______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼװ���о��绯ѧԭ�������з����д������
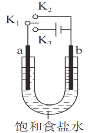
ѡ�� | ���� | �缫���� | ���� | |
a | b | |||
A | K1K2 | ʯī | �� | ģ������������ʴ |
B | K1K2 | п | �� | ģ������������������������������� |
C | K1K3 | ʯī | �� | ģ���ⱥ��ʳ��ˮ |
D | K1K3 | �� | ʯī | ģ�������������ӵ��������������� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ե�ؾ��������ŵ��������ص㣬����õ��㷺Ӧ�ã�п���̼��Ե��������������ҺΪ���Һ������ܷ�ӦʽΪ��Zn��s��+2MnO2��s��+H2O��l��![]() Zn��OH��2��s��+Mn2O3��s�� ����˵��������ǣ� ��
Zn��OH��2��s��+Mn2O3��s�� ����˵��������ǣ� ��
A. ��ع���ʱ��пʧȥ����
B. ��������ĵ缫��ӦʽΪ��2MnO2��s��+H2O��1��+2e��=Mn2O3��s��+2OH����aq��
C. ��ع���ʱ������������ͨ�����·����
D. ���·��ÿͨ��0.2mol���ӣ�п�����������ϼ�С6.5g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaC1O3��NaI�����ʵ���֮��1:1�������ƿ�У�����������������ˮԡ��������Ӧ����NaC1O3��NaIǡ����ȫ��Ӧ������I2��Na2SO4��H2O���������ػ�ɫ������X����XΪ
A. Cl2 B. Cl2O C. Cl2O3 D. ClO2
���𰸡�D
���������������������ת�Ƶ������غ�ã�1molNaI�еĵ�Ԫ����-1�����ɵ��ʵ⣬���ϼ�����ת��1mol���ӣ���NaClO3�е���Ԫ�ػ��ϼ۽���ת��1mol���ӣ���X��������Ԫ�صļ�̬Ϊ+4�ۣ���ѡD.
���㣺������ԭ��Ӧ
�����͡���ѡ��
��������
25
����Ŀ����4.48LCO2ͨ��һ�����Ĺ���������ƺ��ռ���3.36L����(����IJ������ڱ�״����)�������������������
A. 3.2g B. 4.8g C. 5.4g D. 6g
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com