
下列图示与对应的叙述相符的是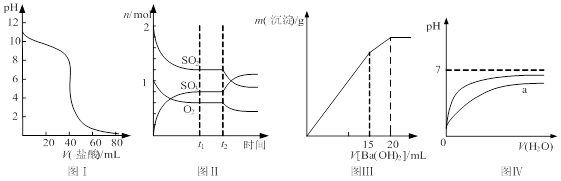
| A.图Ⅰ表示盐酸滴加到0.1 mol/L某碱溶液得到的滴定曲线,用已知浓度盐酸滴定未知浓度该碱时最好选取酚酞作指示剂 |
B.图Ⅱ表示一定条件下进行的反应2SO2+O2 2SO3 各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 2SO3 各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 |
| C.图Ⅲ表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20 mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
| D.图Ⅳ表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是盐酸 |
B
解析试题分析:A.人的视觉有滞后性,为了减少滴定误差,选择指示剂时滴定终点的颜色变化从浅到深,这样误差较小。用已知浓度盐酸滴定未知浓度该碱时最好选取甲基橙作指示剂。错误。B.反应在t2时刻SO2和O2浓度减小,而SO3的浓度增大,化学平衡正向移动,由于该反应的正反应是气体体积减小的反应,所以改变的条件可能是缩小容器体积,使容器内的气体压强增大,平衡正向移动。正确。C向某明矾溶液中加入Ba(OH)2溶液,当Al3+沉淀完全时发生反应:2KAl(SO4)2+3Ba(OH)2=K2SO4+ 2Al(OH)3↓ +3BaSO4↓,当SO42-沉淀完全是发生反应:KAl(SO4)2+2Ba(OH)2=KAlO2+2BaSO4↓+2H2O。所以在加入15mlBa(OH)2溶液时铝离子恰好沉淀完全;在加入20 mL Ba(OH)2溶液时硫酸根离子恰好沉淀完全。错误。D.向pH相同的盐酸与醋酸中分别加入等体积的水时,由于在醋酸溶液中存在醋酸分子会继续电离产生H+,因此醋酸溶液的pH变化较小。故其中曲线a对应的是醋酸,曲线b对应的是盐酸。错误。
考点:考查图像法在酸碱中和滴定、平衡移动、沉淀反应及电解质溶液稀释中的应用的知识。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:单选题
有4种金属a、b、c、d,它们与浓HNO3反应时,只有a不反应;往这4种金属粉末的混合物中加入盐酸,其中b、c溶解,过滤后,在滤液中加入过量的NaOH溶液,可得到c离子的沉淀,则这4种金属的活动性强弱的顺序可能是
| A.c > b > d > a | B.b > a > d > c | C.a > b > c > d | D.d > c > b > a |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断下列说法错误的是( )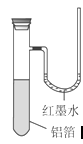
| A.实验中发生的反应都是氧化还原反应 |
| B.铝是一种较活泼的金属 |
| C.铝与氧气反应是放热反应 |
| D.铝片上生成的白毛是氧化铝和氧化汞的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列化学实验事实及其结论都正确的是( )
| 选项 | 实验事实 | 结论 |
| A | 将SO2通入含HClO的溶液中生成H2SO4 | HClO的酸性比H2SO4强 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | 稀、浓硝酸分别与铜反应,还原产物分别为NO和NO2 | 稀硝酸氧化性比浓硝酸强 |
| D | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列现象或事实可用同一原理解释的是
A氯化铵晶体和碘晶体加热都产生气体
B.明矾和液氯都可用于处理生活用水
C.漂白粉和过氧化钠都可用于漂白有色织
D.常温下,铁和铜分别放在浓硫酸中都无明显现象
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
为测定某镁铝合金样品中铝的含量,进行了下列实验:取一定量合金,加入100 mL 0.3 mol·L-1稀硫酸,合金完全溶解,产生的气体在标准状况下体积为560 mL;再加入0.2 mol·L-1 NaOH溶液至沉淀质量恰好不再变化,用去350 mL NaOH溶液。则所取样品中铝的物质的量为
| A.0.005 mol |
| B.0.010 mol |
| C.0.020 mol |
| D.0.030 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
证明某溶液只含有Fe2+而不含有Fe3+的实验方法是
| A.先滴加氯水,再滴加KSCN溶液后显红色 |
| B.先滴加KSCN溶液,不显红色,再滴加氯水后显红色 |
| C.滴加NaOH溶液,先产生白色沉淀,后变为灰绿色,最后呈红褐色 |
| D.只需滴加KSCN溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com