
���� NaͶ��CuSO4��Һ��ʱ�����Ⱥ�ˮ��Ӧ����NaOH��H2�����ɵ�NaOH�ٺ�CuSO4���ֽⷴӦ������ɫ������ͭ�������Դ������
��� �⣺NaͶ��CuSO4��Һ��ʱ�����Ⱥ�ˮ��Ӧ����NaOH��H2�����ɵ�NaOH�ٺ�CuSO4���ֽⷴӦ������ɫ������ͭ�����������Ļ�ѧ��Ӧ����ʽΪ2Na+CuSO4+2H2O=Cu��OH��2��+Na2SO4+H2������
��1���Ƹ���Һ���ϣ���֪�Ƶ��ܶ�С������ͭ��Һ���ܶȣ�
��2���ۻ���������С��֪����ˮ��Ӧ���ų�����ʹ���ۻ���
��3���Ĵ��ζ������������������ʧ����֪��Ӧ���ҷų����壬�����������ƶ�С���Ĵ��ζ���
��4����Һ�в�����ɫ��״��������֪����ˮ��Ӧ�����������ƣ�������ͭ��Ӧ����������ͭ��ɫ��״������
�ʴ�Ϊ���Ƹ���Һ���ϣ��Ƶ��ܶ�С������ͭ��Һ���ܶȣ��ۻ���������С������ˮ��Ӧ���ų�����ʹ���ۻ����Ĵ��ζ������������������ʧ����Ӧ���ҷų����壬�����������ƶ�С���Ĵ��ζ�����Һ�в�����ɫ��״����������ˮ��Ӧ�����������ƣ�������ͭ��Ӧ����������ͭ��ɫ��״������
���� ���⿼���ƵĻ�ѧ���ʣ�Ϊ��Ƶ���㣬��������ˮ�ķ�ӦΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��Ԫ�ػ�����֪ʶ��Ӧ�ã���Ŀ�ѶȲ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �����£���pH��ֽ�ⶨŨ��Ϊ0.1mol•L-1 NaClO��Һ��pH | |
| B�� | ��4mL0.01mol•L-1 KSCN��Һ��1mL0.01mol•L-1 FeCl3��Һ��ֻ�ϣ��ټ�������KSCN��Һ����Һ��ɫ���֤����Һ�д���ƽ�⣺��Fe3++3SCN-?Fe��SCN��3 | |
| C�� | �����ϡ��Һ�����������ϡ��Һ�У����ⷴӦ����Һ�¶�ֵƫС | |
| D�� | �ⶨNa2SO3��Һ��Na2CO3��Һ������ԣ�˵���ǽ����ԣ�S��C |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 483.6 kJ•mol-1 | B�� | 241.8 kJ•mol-1 | C�� | 571.6 kJ•mol-1 | D�� | 285.8 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
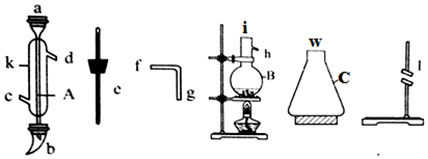
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl3��Һ��Cu��Ӧ��Fe3++Cu�TFe2++Cu2+ | |
| B�� | AgNO3��Һ��NaCl��Ӧ��Ag++Cl-�TAgCl�� | |
| C�� | Cu��OH��2��CH3COOH��Ӧ��OH-+H+�TH2O | |
| D�� | CaCO3��HNO3��Ӧ��CO32-+2H+�TH2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�1 mol CO2��CO�Ļ�����к��е���ԭ����Ϊ1.5NA | |
| B�� | ��״���£�11.2LCCl4�����ķ�����Ϊ0.5 NA | |
| C�� | 25�棬1.01��105Pa��66gCO2������ԭ����Ϊ4.5NA | |
| D�� | 1 mol•L-1 CuCl2��Һ�к��е���������Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ֱ��ʾN2��H2��NH3������������ڹ����������ϳɰ��Ĺ��̿���ͼ1��ʾ��
�ֱ��ʾN2��H2��NH3������������ڹ����������ϳɰ��Ĺ��̿���ͼ1��ʾ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com