为探究Fe(NO
3)
2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究性学习:
【查阅资料】金属活泼性不同,其硝酸盐分解产物不同。
(1)K→Na活泼金属的硝酸盐分解生成亚硝酸盐和氧气;
(2)Mg→Cu等较活泼金属的硝酸盐分解生成氧化物、NO
2和O
2;
(3)Hg以后不活泼金属的硝酸盐分解生成金属单质、NO
2和O
2。
2KNO
3
2KNO
2↑+O
2↑
2Cu(NO
3)
2
2CuO+4NO
2↑+O
2↑
2AgNO
3
2Ag+2NO
2↑+O
2↑
【实验一】探究Fe(NO
3)
2热分解固体产物中Fe元素的价态。该小组甲同学将其溶于足
量的稀H
2SO
4得到相应两份溶液,进行以下探究实验。
【提出猜想】猜想一:Fe元素只显+2价;
猜想二:Fe元素只显+3价;
猜想三:Fe元素____
_____。
【实验操作】①向一份溶液中滴入KSCN溶液②将稀酸性KMnO
4溶液中滴入另一份溶液
【实验现象】实验①
;实验②
。
【实验结论】猜想二成立,则Fe(NO
3)
2分解的化学方程式是
。
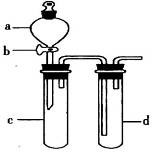
【实验二】探究Fe(NO
3)
2热分解气体产物的性质。小组乙、丙同学进行了如下图所示的实验(收集时操作恰当,几乎没有空气)

实验步骤:①连接仪器;②检查装置气密性;③取一定质量Fe(NO
3)
2装于大试管,并重
新连接好仪器;④加热;⑤……
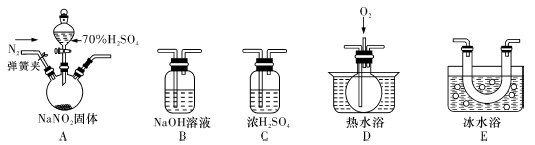
(1)乙同学使用A装置收集气体,恰好收集到常温常压下27mL的红棕色气体,为确保数据的准确性,读数时必须
。
(2)乙同学用带火星木条检验量筒内气体时,发现木条燃烧,且颜色变浅甚至无色,下列判断中正确的是
。
a.气体中只有NO
2 b.气体是O
2、NO
2的混合物
c.支持燃烧的气体只有O
2 d.NO
2支持燃烧
(3)丙同学取等质量的Fe(NO
3)
2使用B装置收集气体,可收集到
mL气体。
【实验三】探究固体混合物的成分。小组丁同学取KNO
3、Cu(NO
3)
2、Fe(NO
3)
2的混合粉末充分加热后用排水法未收集到任何气体,则KNO
3、Cu(NO
3)
2、Fe(NO
3)
2的物质的量之比可能是( )
| A.1:2:2 | B.2:1:3 | C.1:2:3 | D.3:8:6 |



 2KNO2↑+O2↑
2KNO2↑+O2↑ 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑  2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑