
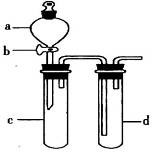
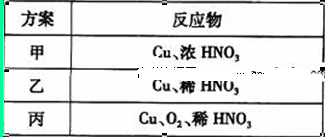
 2CuO,CuO+2HNO3=Cu(NO3)2+H2O,从过程可以看出该过程不会产生有毒气体,环保且没有多消耗原料,故答案为:丙;耗酸量最少,无污染;(4)根据氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,利用KMnO4与浓盐酸反应:2KMnO4KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,说明KMnO4氧化性强于Cl2,再利用产生的氯气与KBr溶液反应得到溴:Cl2+2KBr=2KCl+Br2,说明Cl2氧化性强于Br2,所以c中有黄绿色气体产生,d中溶液变为黄棕色,同时要注意尾气吸收,故答案为:c中有黄绿色气体产生,d中溶液变为黄棕色;证明氧化性KMnO4>Cl2>Br2;没有处理尾气。
2CuO,CuO+2HNO3=Cu(NO3)2+H2O,从过程可以看出该过程不会产生有毒气体,环保且没有多消耗原料,故答案为:丙;耗酸量最少,无污染;(4)根据氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,利用KMnO4与浓盐酸反应:2KMnO4KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,说明KMnO4氧化性强于Cl2,再利用产生的氯气与KBr溶液反应得到溴:Cl2+2KBr=2KCl+Br2,说明Cl2氧化性强于Br2,所以c中有黄绿色气体产生,d中溶液变为黄棕色,同时要注意尾气吸收,故答案为:c中有黄绿色气体产生,d中溶液变为黄棕色;证明氧化性KMnO4>Cl2>Br2;没有处理尾气。

科目:高中化学 来源:不详 题型:单选题
| A.将固体加热,用湿润的红色石蕊试纸在试管口检验,看是否变蓝 |
| B.加水溶解,用PH试纸测溶液的酸碱性 |
| C.加入NaOH溶液,加热,再滴入酚酞试液 |
| D.加入NaOH溶液,加热,用湿润的红色石蕊试纸在试管口检验,看是否变蓝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
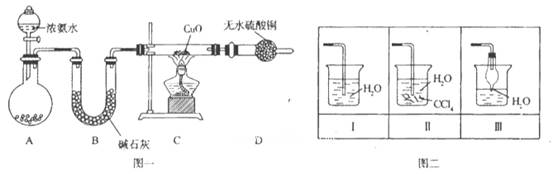
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
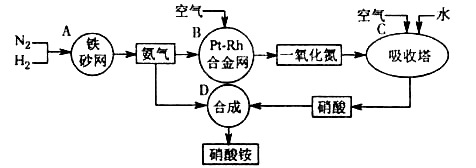
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.所含四种元素的原子半径由小到大的顺序为:H<O<N<C |
| B.同周期的三种元素的得电子能力由大到小的顺序为: O>N>C |
| C.除去NaCl固体中混有少量的NH4HCO3固体可以采用加热的方法 |
D.其与足量氢氧化钠溶液共热的离子方程式为:NH4++OHˉ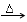 NH3↑+H2O NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜片完全消耗时所用的时间 | B.反应中转移的电子总数 |
| C.反应所消耗硝酸的物质的量 | D.反应生成气体的体积(标准状况) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1 | B.0.12 | C.0.15 | D.0.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com