
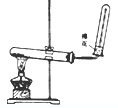
| A、氯气 | B、氧气 | C、氨气 | D、氢气 |
 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
| 酸 | 电离平衡常数K |
| CH3COOH | 1.76×10- |
| H2CO3 | K1=4.31×10-7 K2=5.61×10-1 |
| H3PO4 | K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过量新制的氯水滴到蓝色的石蕊试纸上,试纸先变红,说明氯水中含有H+ |
| B、向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- |
| C、向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ |
| D、氯水能使有色花瓣褪色,说明氯水中含有Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定含有CO2、H2O蒸气,可能含有H2、CO |
| B、一定含有H2O蒸气、CO,可能含有CO2、H2 |
| C、一定含有CO2、CO,可能含有H2O蒸气、H2 |
| D、一定含有CO、H2,可能含有H2O蒸气、CO2中的1种或2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钠固体应密封贮存于塑料瓶中 |
| B、碘固体保存在棕色细口瓶中 |
| C、氯水贮存在棕色细口瓶中 |
| D、溴存放在试剂瓶里,并往瓶中加一些水进行液封 |
查看答案和解析>>
科目:高中化学 来源: 题型:
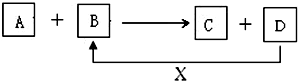 A、B、C、D、X均为中学化学常见的物质.它们之间存在如图所示转化关系(图中反应条件略去)
A、B、C、D、X均为中学化学常见的物质.它们之间存在如图所示转化关系(图中反应条件略去)查看答案和解析>>
科目:高中化学 来源: 题型:
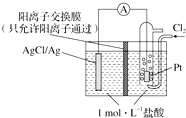
| A、当电路中转移0.1 mol e-时,交换膜左侧溶液中约减少0.2 mol离子 |
| B、放电时,交换膜两侧溶液中均有大量白色沉淀生成 |
| C、若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D、正极反应为AgCl+e-═Ag+Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com