
��11�֣�����ֲ���纣���������к��зḻ�ĵ�Ԫ�أ���Ԫ���Ե����ӵ���ʽ���ڡ�ʵ������Ӻ�������ȡ�����������(��֪2KI��Cl2===2KCl��I2��������һ���������л��ܼ�)��
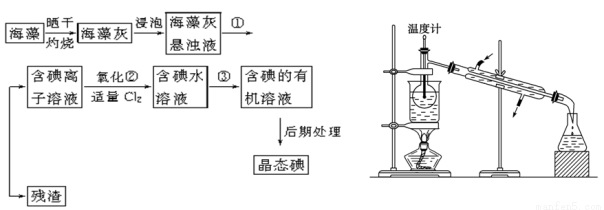
��1��ָ����ȡ��Ĺ������йص�ʵ��������ƣ���________����________��
��2����ȡ��Ĺ����У��ɹ�ѡ����л��Լ���________��
A���� B�����Ȼ�̼ C���ƾ�
��3��Ϊʹ���������к���������Һת��Ϊ����л���Һ��ʵ���������ձ����������Լ���Ҫ�ļг���������ȱ�ٵIJ��������� ��
��4���Ӻ�����л���Һ����ȡ��ͻ����л��ܼ������辭������ָ����ͼ��ʾʵ��װ���еĴ���֮����
�� ��
�� ��
�� ��
��5�����������������ʱʹ��ˮԡ��ԭ���� ��
��6�����Ȼ�̼��____ɫҺ�塣�����ʵ���ñ�����ȡ�������ϲ�Һ�����ɫΪ ɫ���²�Һ�������ʵ���Ҫ�ɷ�Ϊ___________��д��ѧʽ����
��11�֣�ÿ��1�֣�
��1������ �� ��ȡ ��2��AB ��3����Һ©��
��4������ʱû�е�ʯ�������¶ȼ�λ�ô�������ˮ�����ڷ������
��5�����Ⱦ��ȣ��¶Ƚϵ������ƣ�
��6���ޣ��Ϻ�ɫ����ɫ�� KCl
��������
�����������1��������ͼ������ҵ�����Һͨ�������ٵõ�����������Һ�Ͳ�����������Ϊ���ˣ�����ˮ��Һͨ�������ڵõ�������л���Һ����֪������Ϊ��ȡ����2����ȡѡ�õ��ܼò������ˮ��Ӧ��Ҳ��������ˮ���л��ܼ��б������Ȼ�̼������ѡ�þƾ����ƾ�����ˮ����3����ȡ����Ӧ�÷�Һ©�����з�Һ����4���ձ�������ϴ���Ӧ����ʯ�������¶ȼ�ˮ����λ��Ӧ��������ƿ֧�ܿڲ����������¶ȣ������ܵ���ȴˮӦ�������������������ڷ������5�������������������Ȼ�̼���л��ܼõķе�ϵͣ�Ϊ�����Ⱦ��ȣ������¶ȣ�Ӧ����ˮԡ���ȡ���6�������ܶȱ�ˮС����ȡ���ϲ����л��㣬���ڱ��г��Ϻ�ɫ���²���ˮ�㣬������Ҫ���Ȼ��ס�
���㣺��������ȡ���ʵ�飬�����ˡ���ȡ������Ȳ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ����������и߶���ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ijϩ���������ӳɺ�õ�2,2���������飬��ϩ����������
A��2,2��������3����ϩ B��2,2��������2����ϩ
C��2,2��������1����ϩ D��3,3��������1����ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ����������и߶��ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ��Ӧ�����ӷ���ʽ��д��ȷ����
A������ͨ���Ȼ�������Һ�У�Fe2+��Cl2==2Cl����Fe3+
B��������ˮ��Ӧ��Cl2 + H2O==Cl��+ ClO�� + 2H+
C��ͭ��ϡ���ᷴӦ��3Cu + 8H+ + 2NO ==3Cu2+ + 2NO�� + 4H2O
==3Cu2+ + 2NO�� + 4H2O
D.���Ȼ����м�������İ�ˮ��Al3++4 NH3��H2O = AlO2�� +4NH4+ + 2 H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�߶���ѧ�����п����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���Ѿ��ﵽƽ��ķ�Ӧ 2X(g) + Y(g)  2Z(g) ��H<0 ������˵����ȷ����
2Z(g) ��H<0 ������˵����ȷ����
A����С��������������淴Ӧ���ʶ�����ƽ�����淴Ӧ�����ƶ�
B�����߷�Ӧ�¶ȣ��÷�Ӧ��ƽ�ⳣ������
C��������������Խ��ͷ�Ӧ����Ļ�ܣ������ı䷴Ӧ�Ħ�H
D���ı�����ʹƽ�������ƶ�����Ӧ���ת����һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�������
��6�֣���ͭ����Ҫ�ɷ�CuFeS2������ȡͭ����Ҫԭ��
��1��ȡ12.5g��ͭ����Ʒ�����ⶨ��3.60g�����ʲ�����������CuFeS2����Ϊ ��
��2����֪ ��¯����������Cu2S��1200������¼�����Ӧ��
��¯����������Cu2S��1200������¼�����Ӧ��
2Cu2S + 3 O2  2Cu2O + 2 SO2 ��2Cu2O + Cu2S
2Cu2O + 2 SO2 ��2Cu2O + Cu2S  6Cu + SO2
6Cu + SO2
�ٶ�������Ӧ����ȫ��������м��㣺
����6 mol CuFeS2����6 mol Cu��������O2�����ʵ�����
��6 mol CuFeS2��14.25 mol O2��Ӧ�������Ͽɵõ�����Ħ��ͭ��
��6 mol CuFeS2��15.75 mol O2��Ӧ�������Ͽɵõ�����Ħ��ͭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��0.2mol��L-1Ba(OH)2��Һ��0.05mol��L-1NaHSO4��Һ�������Ϻ����м�������Ũ�ȴ�С˳����ȷ����
A��c(Ba2+)��c(OH��)��c(Na+)��c(SO42��)
B��c(Na+)��c(OH��)��c(Ba2+)��c(SO42��)
C��c(Na+)��c(Ba2+)��c(OH��)��c(SO42��)
D��c(OH��)��c(Ba2+)��c(Na+)��c(SO42��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ǿ������Һ�У������������ܴ�����������ҺΪ��ɫ������
A��Ag+��Na+��Cl����K+
B��Na+��Cu2+��SO42����NO3��
C��Mg2+��Na+��SO42����Cl��
D��Ba2+��HCO3����NO3����K+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�¶�ʱ��Ũ�ȶ���1mol/L����������X2��Y2�����ܱ������з������淴Ӧ��������Z����ַ�Ӧ��X2��Ũ��Ϊ0��4mol/L��Y2��Ũ��Ϊ0��8mol/L�����ɵ�Z��Ũ��Ϊ0��4mol/L����÷�Ӧ�Ļ�ѧ����ʽ(Z��X��Y��ʾ)��
A��X2+2Y2 2XY2 B��2X2+Y2
2XY2 B��2X2+Y2 2X2Y
2X2Y
C��X2+3Y2 2XY3 D��3X2+Y2
2XY3 D��3X2+Y2 2X3Y
2X3Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������人�������и߶�10���¿���ѧ���������Ծ��������棩 ���ͣ�ѡ����
����xA(g)+yB(g)  zC(g)+wD(g)��ƽ����ϵ�����¶�����ʱ����ϵ��ƽ����Է���������26��Ϊ29��������˵����ȷ���ǣ� ��
zC(g)+wD(g)��ƽ����ϵ�����¶�����ʱ����ϵ��ƽ����Է���������26��Ϊ29��������˵����ȷ���ǣ� ��
A��x+y>z+w, ����Ӧ�Ƿ��ȷ�Ӧ B��x+y>z+w������Ӧ�����ȷ�Ӧ
C��x+y<z+w���淴Ӧ�Ƿ��ȷ�Ӧ D�� x+y>z+w���淴Ӧ�����ȷ�Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com