
(6分)黄铜矿(主要成分CuFeS2)是提取铜的主要原料
(1)取12.5g黄铜矿样品,经测定含3.60g硫(杂质不含硫),矿样中CuFeS2含量为 。
(2)已知 (炉渣),产物Cu2S在1200℃高温下继续反应:
(炉渣),产物Cu2S在1200℃高温下继续反应:
2Cu2S + 3 O2  2Cu2O + 2 SO2 ;2Cu2O + Cu2S
2Cu2O + 2 SO2 ;2Cu2O + Cu2S  6Cu + SO2
6Cu + SO2
假定各步反应都完全,完成下列计算:
①由6 mol CuFeS2生成6 mol Cu,求消耗O2的物质的量。
②6 mol CuFeS2和14.25 mol O2反应,理论上可得到多少摩尔铜?
③6 mol CuFeS2和15.75 mol O2反应,理论上可得到多少摩尔铜?
(6分)
(1)82.8% (2)①CuFeS2  Cu+FeO+2SO2
Cu+FeO+2SO2 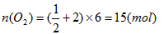
② O2不足量 Cu2S+O2 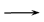 2Cu+SO2 , n(Cu)=6-2(15-14.25)= 4.5 (mol)
2Cu+SO2 , n(Cu)=6-2(15-14.25)= 4.5 (mol)
③O2过量 2Cu2S+3O2 → 2Cu2O+2SO2 ,n(Cu)=6(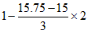 )=3 (mol)
)=3 (mol)
【解析】
试题分析:(1)12.5g黄铜样品中含CuFeS2的质量为3.6g÷(32g/mol×2)×184g/mol=10.35g, 矿样中CuFeS2含量为10.35g/12.5g×100%=82.8% 。
(2)①设消耗O2的物质的量为x
2CuFeS2 +5O2→2Cu+2FeO+4SO2
2mol 5mol 2mol
6 mol x
2mol:6mol=5mol:x ,解得x=15mol
答消耗O2的物质的量15。
②6 mol CuFeS2和14.25 mol O2反应,氧气不足,
2CuFeS2 +4O2→Cu2S+2FeO+3SO2
2mol 4mol 1mol
6mol 12mol 3mol
氧气乘余14.25mol-12mol=2.25mol
设生成Cu ymol由2Cu2S + 3 O2 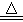 2Cu2O + 2 SO2 ;2Cu2O + Cu2S
2Cu2O + 2 SO2 ;2Cu2O + Cu2S  6Cu + SO2知
6Cu + SO2知
Cu2S+O2=2Cu+SO2
1mol 2mol
2.25mol y
1:2.25=2:y 解得y=4.5mol
答:理论上可得到4.5mol铜?
③6 mol CuFeS2和15.75 mol O2反应,氧氧过量,在第一步反应后氧气乘余
15.75mol-12mol=3.75mol
2Cu2S + 3 O2  2Cu2O + 2 SO2
2Cu2O + 2 SO2
2mol 3mol
2.5mol 3.75mol
乘余Cu2S 的物质的量3mol-2.5mol=0.5mol
设理论上可得到zmol铜?
2Cu2O + Cu2S  6Cu + SO2
6Cu + SO2
1mol 6mol
0.5mol zmol
1mol:0.5mol=6mol:zmol ,解得z=3mol ,
答:理论上可得到3摩尔铜?
考点:质量分数,通过黄铜矿进行关于氧化还原反应方程的计算


科目:高中化学 来源:2014-2015学年湖南益阳市高二上学期10月月考化学试卷(解析版) 题型:选择题
某烃结构式用键线式表示为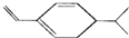 , 该烃与Br2加成时(物
, 该烃与Br2加成时(物
质的量之比为1:1),所得产物有
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北鄂州市高二上第一次月考化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同
B.常温下,2A(s)+B(g)=2C(g)+D(g)不能自发进行,该反应焓变一定大于零
C.1mol硫酸与1molBa(OH)2完全中和所放出的热量为中和热
D.在25℃、101KPa时,2mol S的燃烧热是1mol S的2倍
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省高二上学期期中考试试化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度
B.常温下,向Mg(OH)2饱和溶液中加入NaOH溶液,Mg(OH)2的Ksp不变
C.带有“盐桥”的铜锌原电池比不带“盐桥”的铜锌原电池电流持续时间长
D.对滴加酚酞的NaHCO3溶液加热,红色加深,是因为加热时NaHCO3分解生成Na2CO3,碱性增强
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省高二上学期期中考试试化学试卷(解析版) 题型:选择题
根据生活经验,判断下列物质按酸碱性的一定顺序依次排列正确的是
A.厕所清洁剂 醋 肥皂 厨房清洁剂
B.醋 厕所清洁剂 肥皂 厨房清洁剂
C.厕所清洁剂 厨房清洁剂 醋 肥皂
D.厨房清洁剂 醋 肥皂 厕所清洁剂
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省高一上学期期中化学试卷(解析版) 题型:实验题
(11分)海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下(已知2KI+Cl2===2KCl+I2,碘与溴一样易溶于有机溶剂):
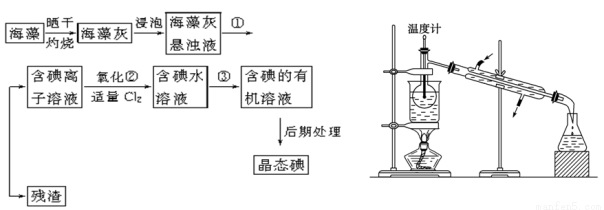
(1)指出提取碘的过程中有关的实验操作名称:①________,③________。
(2)提取碘的过程中,可供选择的有机试剂是________。
A.苯 B.四氯化碳 C.酒精
(3)为使上述流程中含碘离子溶液转化为碘的有机溶液,实验室里有烧杯、玻璃棒以及必要的夹持仪器,尚缺少的玻璃仪器是 。
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出上图所示实验装置中的错误之处:
① 。
② 。
③ 。
(5)进行上述蒸馏操作时使用水浴的原因是 。
(6)四氯化碳是____色液体。如果本实验用苯做萃取剂,则上层液体的颜色为 色,下层液体中溶质的主要成分为___________(写化学式)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省高一上学期期中化学试卷(解析版) 题型:选择题
已知2Fe2++Br2=2Fe3++2Br-。向100mL的FeBr2溶液中通入标准状况下的Cl2 3.36L,充分反应后测得溶液中Cl-与Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为
A.2 mol/L B.1 mol/L C.0.4 mol/L D.0.2 mol/L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省高二上学期期中考试化学试卷(解析版) 题型:选择题
25℃时,下列有关溶液中微粒的物质的量浓度关系错误的是
A.0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-)
B.0.1mol/LNH4Cl与0.1mol/L氨水溶液等体积混合:c(NH3·H2O)>c(NH4+)>c(Cl-)>c(OH-)
C.0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3)
D.Na2C2O4溶液与HCl溶液等体积混合(H2C2O4是二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北武汉新洲三中高二10月月考化学(A卷)试卷(解析版) 题型:选择题
对于可逆反应:2A(g)+B(g) 2C(g);△H<0,下列各图中正确的是( )
2C(g);△H<0,下列各图中正确的是( )
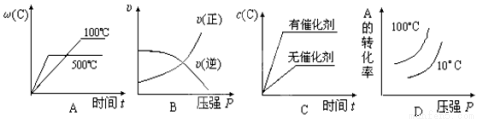
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com