
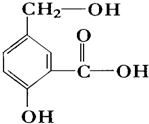
 在某有机物A的分子中,具有酚羟基、醇羟基、羟基等官能团,其结构简式如图.
在某有机物A的分子中,具有酚羟基、醇羟基、羟基等官能团,其结构简式如图.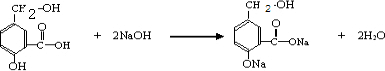 ,
, ;
; ,
, ;
;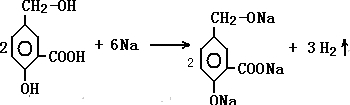 ,
, .
.


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
| A、22.4LNe含有NA个Ne分子 |
| B、0.1mol/LNa2SO4溶液中有0.2NA个Na+ |
| C、25℃,1标准大气压下,22gCO2中含有0.5NA个二氧化碳分子 |
| D、标准状况下,NA个水分子所占的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | M层上电子数是K层的2倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
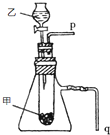 A、B、C、D、E、F为原子序数依次增大的前20号元素,已知A有多种核素,其中一种没有中子,B和C,C和E分别相邻,D的次外层电子数是最外层电子数的两倍.B、E、F的最外层电子数之和为12.
A、B、C、D、E、F为原子序数依次增大的前20号元素,已知A有多种核素,其中一种没有中子,B和C,C和E分别相邻,D的次外层电子数是最外层电子数的两倍.B、E、F的最外层电子数之和为12.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由①式可知H2的燃烧热为241.8KJ/mol |
| B、2H2(g)+O2(g)═2H2O(l)△H>-483.6kJ/mol |
| C、将含1mol NaOH的稀溶液与0.05mol浓硫酸溶液混合后放出的热量为57.3kJ |
| D、将含1mol Ba(OH)2的稀溶液与含2molHCl的稀溶液混合后放出的热量等于114.6kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、9.0 mol?L-1 |
| B、10.0 mol?L-1 |
| C、13.0 mol?L-1 |
| D、14.0 mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com