
 CO32-+H3O+
CO32-+H3O+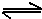 H2CO3+OH-,故B错误;
H2CO3+OH-,故B错误;

科目:高中化学 来源: 题型:阅读理解


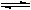 NH4++NH2-
NH4++NH2-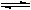 NH4++NH2-
NH4++NH2-查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温 |
| c12(HCl) |
| c3(SiCl4)c2(N2)c6(H2) |
| c12(HCl) |
| c3(SiCl4)c2(N2)c6(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
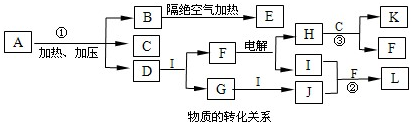
用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g)+2N2(g)+6H2(g)![]() Si3N4(s)+12HCl(g)+Q(Q>0)
Si3N4(s)+12HCl(g)+Q(Q>0)
完成下列填空:
31.在一定温度下进行上述反应,若反应容器的容积为2 L,3 min后达到平衡,测得固体的质量增加了2.80 g,则H2的平均反应速率___ mol/(L·min);该反应的平衡常数表达式K=_____
32.上述反应达到平衡后,下列说法正确的是_。
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si3N4物质的量平衡向左移动
d.其他条件不变,增大HCl物质的量平衡向左移动
33.一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是__。
a.3v逆(N2)=v正(H2) b.v正(HCl)=4v正(SiCl4)
c.混合气体密度保持不变 d.c(N2):c(H2):c(HCl)=1:3:6
34.若平衡时H2和HCl的物质的量之比为![]() ,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比___
,保持其它条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比___![]() (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高二上学期期中考试化学试卷(解析版) 题型:填空题
用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件, 能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅, 其反应如下: 3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g) ΔH <0
Si3N4(s)+12HCl(g) ΔH <0
完成下列填空:
(1)在一定温度下进行上述反应, 若反应容器的容积为2 L, 3 min后达到平衡, 测得固体质量增加了2. 80 g, 则转移电子的物质的量为 ,H2的平均反应速率为 mol/(L·min); 该反应的平衡常数表达式K= 。
(2)上述反应达到平衡后, 下列说法正确的是 。
a. 其他条件不变, 压强增大, 平衡常数K减小
b. 其他条件不变, 温度升高, 平衡常数K减小
c. 其他条件不变, 增大Si3N4物质的量,平衡向左移动
d. 其他条件不变, 增大HCl物质的量,平衡向左移动
(3)一定条件下, 在密闭恒容的容器中, 能表示上述反应达到化学平衡状态的是 。
A. 3v逆(N2)=v正(H2) B. v正(HCl)=4v正(SiCl4)
C. 混合气体密度保持不变 D. c(N2)∶c(H2)∶c(HCl)=1∶3∶6
(4)若平衡时H2和HCl的物质的量之比为 ,
保持其他条件不变, 降低温度后达到新的平衡时,
H2和HCl的物质的量之比
,
保持其他条件不变, 降低温度后达到新的平衡时,
H2和HCl的物质的量之比  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省盐城市高三上学期学情调研考试化学试卷(解析版) 题型:填空题
(10 分)用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g) + 2N2(g) + 6H2(g) Si3N4(s) +
12HCl(g) △H<0
Si3N4(s) +
12HCl(g) △H<0
(1)在一定温度下进行上述反应,若反应容器的容积为2L,3min后达到平衡,测得固体的质量增加了1.40g,则SiCl4的平均反应速率为 ;该反应的平衡常数表达式为 。
(2)上述反应达到平衡后,下列说法正确的是
a.其他条件不变,温度升高,平衡常数K减小
b.其他条件不变,压强增大,平衡向正反应方向移动
c.其他条件不变,增大SiCl4物质的量,平衡向正反应方向移动
d.其他条件不变,增大Si3N4物质的量,平衡向逆反应方向移动
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是
a.v逆(N2)=3v正(H2) b.v正(HCl)=4v逆(SiCl4)
c.混合气体密度保持不变 d.c(N2):c(H2):c(HCl)=1:3:6
(4)若平衡时H2和HCl的物质的量之比为m/n,保持其他条件不变,降低温度后达到新德平衡时,H2和HCl的物质的量之比 m/n(填“>”“=”或“<”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com