
| A、2mol/L |
| B、3mol/L |
| C、4mol/L |
| D、5mol/L |
| m |
| M |
| n |
| V |
| 5.85g |
| 58.5g/mol |
| 19g |
| 95g/mol |
| 0.5mol |
| 0.1L |


 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
| A、在醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b |
| B、在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
| C、0.2 mol?L-1的盐酸,与等体积水混合后pH=1 |
| D、pH=5.6的CH3COOH与CH3COONa混合溶液中,c(CH3COO-)>c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、Na+、CO32- |
| B、H+、Ag+、NO3- |
| C、H+、OH-、SO42- |
| D、Cl-、Ba2+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熔点:Al2O3>Al |
| B、热稳定性NaHCO3>Na2CO3 |
| C、酸性:H2CO3>H2SiO3 |
| D、氧化性:Br2>Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子数目的多少 |
| B、物质的量浓度相同时,溶液的导电能力 |
| C、在水溶液中是否存在电离平衡 |
| D、电离方程式的写法不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
A、有
| ||
B、有
| ||
C、有
| ||
D、有
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是指物质所含的粒子个数,它是物质的数量单位 |
| B、任何物质的摩尔质量等于它的相对原子质量或相对分子质量 |
| C、0.012kgC原子中的原子数为1mol |
| D、在标准状况下,CH4与CO2混合物22.4L,所含有的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
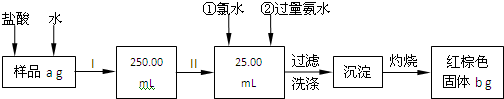
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com