
【题目】已知A、E为金属单质,B是淡黄色粉末且常用于防毒面具中,回答下题。
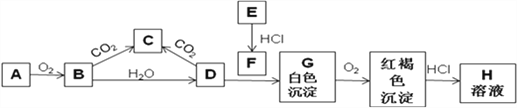
(1)实验室中A常常保存在盛放__________的广口瓶中。
(2)写出B转变成C的化学方程式_______________________。0.1molB参与该反应,转移电子的个数为_________ 。
(3)用化学方程式表示沉淀G颜色发生变化的原因:____________________________________________。
(4)从A、B、C、D、E、G、H选出试剂可制备F,写出对应离子方程式:______________________________________;
(5)直接向F溶液中加入B固体,写出可能出现的现象:______________________________
【答案】 煤油 2Na2O2+2CO2=2Na2CO3+O2 0.1NA 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3 2Fe3++Fe=3Fe2+ 有无色气体生成,产生红褐色沉淀
【解析】(1)实验室中钠常常保存在盛放煤油的广口瓶中。(2)B转变成C的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,反应中过氧化钠既是氧化剂,也是还原剂,则0.1molB参与该反应,转移电子的个数为0.1NA。(3)氢氧化亚铁易被空气中的氧气氧化为氢氧化铁,方程式为4Fe(OH)2 +O2 +2H2O=4Fe(OH)3。(4)可以用氯化铁与铁化合生成氯化亚铁,反应的离子方程式为2Fe3++Fe=3Fe2+;(5)过氧化钠具有强氧化性,溶于水生成氢氧化钠和氧气,则直接向氯化亚铁溶液中加入过氧化钠固体,可能出现的现象是有无色气体生成,产生红褐色沉淀。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣探究小组将一批废弃的线路板简单处理后,得到含Cu(70%)、Al(25%)、Fe(4%)及少量Au等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的流程: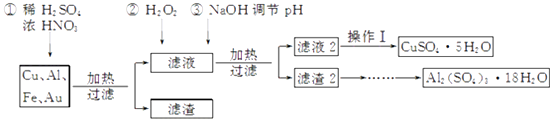
已知:Fe3+、Al3+、Cu2+开始沉淀至沉淀完全的pH范围分别为:2.2~3.2、4.1~5.0、5.3~6.6.
(1)得到滤渣1的主要成分为 .
(2)操作Ⅰ包含的实验步骤有:、冷却结晶、过滤、洗涤、干燥;过滤操作所用到的玻璃仪器有烧杯、玻璃棒和 .
(3)操作Ⅰ中常用无水乙醇对晶体进行洗涤,选用无水乙醇的原因是 .
(4)第②步加H2O2后发生反应的离子方程式为 .
(5)取上述硫酸铝晶体进行热重分析,其热分解主要分为三个阶段:323K~523K,553K~687K,当温度在1 043K以上不再失重,下表列出了不同温度下的失重率:[硫酸铝晶体化学式为Al2(SO4)318H2O,相对分子质量为666]
已知:失重%= ![]() ×100%.
×100%.
温度(K) | 失重(%) | |
第一阶段 | 323~523 | 40.54 |
第二阶段 | 553~687 | 48.65 |
第三阶段 | 1 043以上 | 84.68 |
通过计算确定(写出计算过程):
①失重第一阶段分解产物的化学式;
②失重第二阶段反应的反应化学方程式.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室在常温下将浓盐酸与高锰酸钾混合能够制氣气,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O下列有关该反应的说法正确的是( )
A.KMnO4是还原剂
B.HCl是氧化剂
C.HCl中的氯元素得到电子
D.KMnO4中的Mn元素被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关Na2CO3和NaHCO3的叙述中正确的是( )
A. 相同质量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体质量相同
B. Na2CO3比NaHCO3热稳定性强
C. Na2CO3和NaHCO3均可与澄清石灰水反应
D. Na2CO3和NaHCO3均不可与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.石蕊试纸和pH试纸使用前都必须用蒸馏水润湿
B.沉淀溶解达到平衡时,溶液中溶质的离子浓度相等,且保持不变
C.电离和水解反应都是吸热过程
D.酸式盐的pH均小于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一瓶无色澄清的溶液,可能由以下离子中的几种组成:Na+、K+、NH4+、Fe2+、SO42-、I-、CO32-、Cl-、SO32-、MnO4-,请根据以下实验步骤及现象回答问题:
步骤一:取适量待测液,加入NaOH溶液并加热,得到溶液A,并产生刺激性气味的气体
步骤二:向溶液A加入足量稀盐酸和BaCl2溶液,得到溶液B、白色沉淀和有刺激性气味的气体
步骤三:往B溶液中通入适量Cl2,得到黄褐色溶液C
(1)下列有关该溶液说法正确的是__________。
A. 一定存在SO42-、I-、NH4+、SO32-
B. 一定不存在Fe2+、CO32-、MnO4-
C. 可能存在CO32-、Cl-、Na+、K+
D. 可用AgNO3溶液确认原溶液中是否存在Cl-
(2)步骤三得到黄褐色溶液的离子方程式是____________。
(3)若向原溶液中先加入足量的盐酸,再加入足量的________(填化学式)并加热,通过现象也能得出步骤一、二相同的结论。
(4)对于溶液中还可能存在的阳离子,确认其存在的实验方法是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列题目
(1)现有以下物质 ① 酒精 ②盐酸 ③熔融KCl ④KOH固体 ⑤蔗糖 ⑥铜 ⑦稀H2SO4溶液
以上物质中属于电解质的是(填序号)________________
(2)同温同压下,同体积的CO2和CO,它们的分子数之比为____________ ,密度之比为_____________。
(3)向沸水中逐滴滴加1mol·L-1FeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒直径的范围是___________________。
(4)下列物质:①Cl2;②Na2CO3;③NaHCO3;④K—Na合金;⑤Na。
广泛用于玻璃、造纸的是______________(填编号,下同)
可用作原子反应堆的导热剂的是________________________。
(5)氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):

上述反应中发生了氧化还原反应的是:________(填“a”、“b”、“c”或“e”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2(g)+F2(g)=2HF(g)△H=﹣270kJ/mol,下列说法正确的是( )
A.在相同条件下,1mol H2与1mol F2的能量总和大于2mol HF气体的能量
B.1mol H2与1mol F2反应生成2mol液态HF放出的热量小于270kJ
C.该反应的逆反应是放热反应
D.该反应过程的能量变化可用如图来表示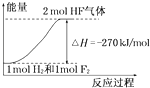
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com