
溶氧分析仪能连续、自动测量水中微量的溶解氧含量,可用于工业锅炉用水,实验室制备除氧水等方面。溶氧分析仪的核心部件是氧传感器,传感器中银做阳极,金做阴极,二电极之间连接一稳定的直流电源,以氯化钾溶液为电解质溶液,电解质溶液与取样水之间有一层氧气可以透过的薄膜,测量金电极上产生的还原电流的大小得出氧气的含量。
⑴ 试写出溶氧分析仪的有关电极反应式
阴极_______________________________,阳极____________________________________
⑵ 请从你写的电极反应式推测影响氧传感器的性能的因素可能有哪些?
在高温下高炉中氧含量的测定可用氧化锆(ZrO2)氧传感器来测定,在氧化锆中加入MgO,Y2O3等立方晶系的氧化物后,在600℃以上高温时成为氧的快离子导体。其导电性能主要源于掺杂晶体中的氧离子空位。下图为氧化锆固体电解质的导电原理。
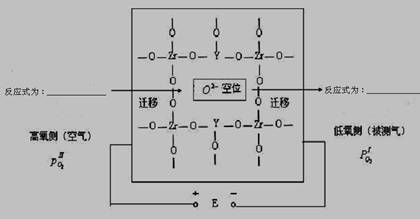
⑶ 写出高氧侧和低氧侧的电极反应式
高氧侧______________________________,低氧侧________________________________
⑷ 若某掺杂电极Y2O3的ZrO2晶体中氧离子空位数为3.01×1020个,则理论上掺杂的Y2O3质量为多少克?
⑴ 阴极反应 O2 + 2H2O + 4e == 4OH-
阳极反应 Ag – e- + Cl- == AgCl (2分 ,各1分)
⑵ pH值,H2S的浓度,重金属离子 (写出二个即可) (2分)
⑶ O2+ 4e - === 2O2- , 2O2- — 4e- === O2 (2分 ,各1分)
⑷ 每掺杂1molY2O3得到的氧离子空位为1mol, 计算得Y2O3质量为:
(3.01X1020/NA) ??M Y2O3 =1.13??10-1g (三位有效数字)(2分)
⑴此问中,一个关键问题是要判断该电化学装置的类型。虽然题中各种描述,该装置是电解池,但是从测量原理等方面来看,这却是一个原电池装置。该装置利用原电池产生的电流对稳定直流电的抵消作用,来测量电流强度,进而确定O2的浓度。因此,在正极,O2+ 2H2O + 4e == 4OH- ,由于O2的浓度不一样,影响了该电对的电极电势。负极Ag失电子,并与Cl-形成沉淀。
⑵影响氧传感器的因素就是影响⑴中两个电极电极电势大小的因素。正极的电势与溶液pH有关,负极由于Ag(Ⅰ)的存在形式会影响到该电极的电极电势,因此影响Ag(Ⅰ)存在形式的因素都会对氧传感器的性能产生影响。
⑶根据题意,该固体电解质中载荷离子为O2-,因此与恒定电流正极相连一侧,即高氧侧,失去电子,产生还原电流,因此电极反应式为:O2+ 4e - === 2O2- 。另一侧O2-得电子生成O2。
⑷氧离子空位的物质的量为3.01×1020/6.02×1023=5.00×10-4(mol),每一个Y3+置换一个Zr4+,正电荷减小1,因此根据电荷守恒原理n(Y)=2n(Y2O3) =5.00×10-4×2 mol,得n(Y2O3)=5.00×10-4 mol,从而求得其摩尔质量。


科目:高中化学 来源: 题型:
| 元素 | A | B | C | D |
| 性质或结构信息 | 单质常温下为固体,难溶于水易于溶CS2.能形成2种二元含氧酸. | 原子的M层有1个未成对的p电子.核外p电子总数大于7. | 单质曾被称为“银色的金子”.与锂形成的合金常用于航天飞行器.单质能溶强酸和强碱. | 原子核外电子层上s电子总数比p电子总数少2个.单质和氧化物均为空间网状晶体,具有很高的熔、沸点. |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 元 素 | M | F | |
| 电能 (kJ?mol-1) |
I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 以任意比互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 化学式 | Fe | FeO | Fe2O3 | Fe3O4 | Fe(OH)2 | Fe(OH)3 |
| 颜色 | 银白色 | 黑色 | 红色 | 黑色 | 白色 | 红褐色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com