
【题目】已知有以下相互转化关系,试回答:

(1)写出B的化学式:__________,C中溶质的化学式:__________,D中溶质的化学式:__________,H的化学式:__________。
(2)写出由E转变成F的化学方程式:__________。
(3)写出由A与盐酸反应转变成B的离子方程式:__________。
(4)向G溶液加入A的离子方程式:__________。
【答案】![]() KOH
KOH![]()
![]()
![]()
![]()
![]()
【解析】
白色沉淀E在空气中变为红褐色沉淀F,则F是氢氧化铁、E是氢氧化亚铁;氢氧化铁与盐酸反应生成G,则G是氯化铁;D与硝酸酸化的硝酸银反应生成白色沉淀H,H是氯化银,所得溶液焰色反应呈紫色,则D中含有K+;D是氯化钾;B与C反应生成氢氧化亚铁和氯化钾,则B是氯化亚铁、C是氢氧化钾;A与盐酸反应生成氯化亚铁和气体,则A是铁单质,气体是氢气。
白色沉淀E在空气中变为红褐色沉淀F,则F是氢氧化铁、E是氢氧化亚铁;氢氧化铁与盐酸反应生成G,则G是氯化铁;D与硝酸酸化的硝酸银反应生成白色沉淀H,H是氯化银,所得溶液焰色反应呈紫色,则D中含有K+;D是氯化钾;B与C反应生成氢氧化亚铁和氯化钾,则B是氯化亚铁、C是氢氧化钾;A与盐酸反应生成氯化亚铁和气体,则A是铁单质,气体是氢气。根据以上分析,(1)B是氯化亚铁,化学式是![]() ,C中溶质的化学式是KOH,D中溶质的化学式是
,C中溶质的化学式是KOH,D中溶质的化学式是![]() ,H是氯化银,化学式是
,H是氯化银,化学式是![]() 。(2)氢氧化亚铁被氧气氧化为氢氧化铁,化学方程式是
。(2)氢氧化亚铁被氧气氧化为氢氧化铁,化学方程式是![]() 。(3)由铁与盐酸反应转变成氯化亚铁和氢气,反应的离子方程式是
。(3)由铁与盐酸反应转变成氯化亚铁和氢气,反应的离子方程式是![]() 。(4)氯化铁溶液加入铁粉生成氯化亚铁,反应的离子方程式是
。(4)氯化铁溶液加入铁粉生成氯化亚铁,反应的离子方程式是![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】金刚石、SiC具有优良的耐磨、耐腐蚀特性,应用广泛。
(1)一定条件下,Na与CCl4可制备金刚石,反应结束冷却至室温后,回收其中的CCl4的实验操作名称为____。推测该反应的类型为____。(填标号)
A..分解反应 B.置换反应 C.氧化还原反应 D.离子反应
(2)已知:Si+2NaOH+H2O===Na2SiO3+2H2↑。在高温电炉中碳和SiO2反应可制得SiC,同时生成CO,其粗产品中杂质为Si和SiO2。
①请写出电炉中所发生反应的化学方程式:___________,每有1 mol SiC生成时,转移电子的物质的量为____。
②现将20.0 g SiC粗产品加入到过量的NaOH溶液中充分反应,收集到0.1 mol氢气,过滤得SiC固体11.4 g,滤液稀释到1 L,则硅酸盐的物质的量浓度为______。
(3)下列关于金刚石、SiC和单质Si的说法不正确的是_____。(填标号)
A.金刚石、SiC和单质Si都属于无机非金属材料
B.金刚石和石墨、晶体硅和无定形硅分别互为同素异形体
C.金刚石和单质硅都是良好的半导体材料
D.金刚石、SiC和Si晶体结构类似
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是学习化学的重要工具,它隐含许多信息和规律。下表所列是五种短周期元素的原子半径及主要化合价(已知铍的原子半径为0.089 nm)。
元素代号 | A | B | C | D | E |
原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
(1)用元素代号标出它们在元素周期表中对应的位置(以下为周期表的一部分)。
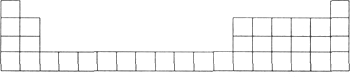
(2)B元素处于周期表中第_______周期第________族。
(3)B的最高价氧化物对应的水化物与C的最高价氧化物对应的水化物反应的离子方程式为_______________。
(4)上述五种元素的最高价氧化物对应水化物酸性最强的是__________(填化学式)。
(5)C、E形成的化合物有__________(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了一种电解法制取Fe(OH)2的实验装置(如图)。通电后,溶液中产生白色沉淀,且较长时间不变色。下列说法中正确的是( )
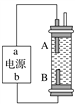
A. 电源中a为负极,b为正极
B. 电解池中的电解液不可以是NaCl溶液
C. B电极发生的反应:2H++2e-===H2↑
D. A、B两端都必须使用铁作电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。
(1)常温下,可用铁或者铝制的容器盛放浓硝酸,说明浓硝酸具有________ 性
A.酸性 B.强氧化性 C.吸水性 D.脱水性
(2)浓H2SO4能够用于干燥某些气体,是由于它具有_____性;下列气体能用浓硫酸来进行干燥的是_____
①Cl2 ②H2S ③CO2 ④NH3 ⑤SO2
(3)浓H2SO4能使纸片变黑,是由于它具有____性;
(4)在加热条件下铜与浓硫酸反应,浓硫酸表现性质为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示一些物质间的从属关系,不正确的是( )
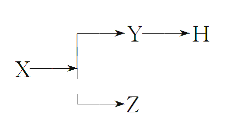
选项 | X | Y | Z | H |
A | 分散系 | 胶体 | 溶液 | 烟 |
B | 电解质 | 酸 | 碱 | 盐 |
C | 元素周期表的纵行 | 主族 | 副族 | 卤族 |
D | 化合物 | 共价化合物 | 离子化合物 | 酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极,e、f是小试管。通电一段时间后,在c、d两极上共收集到336mL(标准状况)气体。
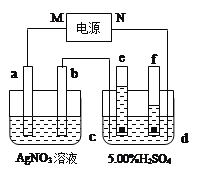
请回答下列问题:
(1)直流电源中,M为_______极。
(2)Pt电极上生成的物质是_______,其质量为______g。
(3)电源输出的电子,其物质的量与电极b、c、d分别生成的物质的物质的量之比为:__________。
(4)AgNO3溶液的浓度________(填增大、减小或不变。下同),H2SO4溶液的pH_________。
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰[(CN)2]的化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间,下列有关反应方程式不正确的是
A. (CN)2和NaOH溶液反应:(CN)2+2OH-=CN-+CNO-+H2O
B. MnO2和HCN反应:MnO2+4HCN(浓)![]() Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
C. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
D. 在NaBr和KCN混合溶液中通入少量Cl2:Cl2+2CN-=2Cl-+(CN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光刻胶是大规模集成电路印刷电路板技术中的关键材料,某一光刻胶的主要成分如图所示,下列有关说法正确的是( )

A. 该物质可经过缩聚反应制得
B. 1 mol该物质可消耗4 mol H2
C. 该物质可稳定存在于碱性溶液中
D. 合成此高聚物的单体的化学式为C11H10O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com