
【题目】下列物质不经过化学变化就能从海水中获得的是( )
A. 单质溴 B. 单质镁 C. 烧碱 D. 食盐
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
【题目】pH=1的某溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种(忽略水的电离及离子的水解),取该溶液进行连续实验,实验过程如下:

下列有关推断不正确的是
A. 沉淀H为AI(OH)3、BaCO3的混合物
B. 根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl-
C. 溶液X中一定含有Al3+、NH4+、Fe2+、SO42-、H+
D. 若溶液X为100mL,产生的气体A为44.8mL(标况),则X中c(Fe2+)=0.06mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器内,800 ℃时反应2NO(g)+O2(g)![]() 2NO2(g) ΔH<0,n(NO)随时间的变化如下表:
2NO2(g) ΔH<0,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
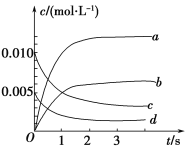
(1)右图中表示NO2的变化的曲线是________。用O2表示从0~2 s内该反应的平均速率v=________。
(2)能说明该反应已达到平衡状态的是________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.容器内密度保持不变
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是________。
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的数值,下列说法中正确的是( )
①0.5molO3与11.2LO2所含的分子数一定相等
②标准状况下,22.4L氯气与足量铁粉充分反应,转移的电子数为3NA
③通常状况下,NA 个CO2分子占有的体积为22.4L
④常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
⑤常温下,4.4g CO2和N2O(不反应)混合物中所含有的原子数为0.3NA
⑥在反应KIO3+6HI═KI+3I2+3H2O中,每生成3molI2转移的电子数为5NA
⑦标准状况下,22.4L SO3含有的分子数为NA
⑧在常温常压下,1mol O2含有的原子数为2NA
⑨物质的量浓度为0.5molL﹣1 MgCl2溶液中,含有Cl﹣个数为NA
⑩将100mL 0.1molL﹣1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数目为0.01NA .
A.①②④⑧
B.③⑥⑨⑩
C.④⑤⑥⑧
D.④⑤⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用.请回答下列问题: 
(1)该“84消毒液”的物质的量浓度约为molL﹣1(小数点后保留一位).
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=molL﹣1 .
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为37.25%的消毒液.需要称量NaClO固体的质量为g
(4)配制上述“84消毒液”时,其正确的操作顺序是(每个操作只用一次): . A.用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.在烧杯中加入适量水溶解
C.将烧杯中的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀,装入贴有标签的试剂瓶
E.改用胶头滴管加水,使溶液的凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
G.用天平称量该物质
(5)在溶液配制过程中,下列操作使溶液浓度偏小的是: .
A.定容时仰视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的“84消毒液”而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,再用胶头滴管加水至刻度线.
E.转移溶液时未洗涤烧杯.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中说明乙醇作为燃料的优点的是
①燃烧时发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量热量
A.②③④B.①②③C.①②④D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大家都知道,H2S、SO2、NO和CO都是常见的大气污染物,治理污染优化环境对人类的生产与生活尤为重要。
(1)H2S和SO2都是来自硫酸工业的污染物,下列说法正确的是___________。
A .两气体均可以用浓硫酸来干燥 B. 两气体可以用溴水来鉴别
C. 两气体均可以用氢氧化钠溶液来吸收 D. SO2使KMnO4溶液褪色表现出漂白性
(2)汽车尾气的主要成分是氮的氧化物和CO,目前用在汽车的排气管上安装催化转化装置,发生反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) 来除去这两种污染物。有人设想按下列反应:2CO(g)=2C(s)+O2(g)来除去CO,已知该反应为吸热反应,则该设想能否实现___选填“能”或“不能”),理由是_______________________________________。
N2(g)+2CO2(g) 来除去这两种污染物。有人设想按下列反应:2CO(g)=2C(s)+O2(g)来除去CO,已知该反应为吸热反应,则该设想能否实现___选填“能”或“不能”),理由是_______________________________________。
(3)为减少SO2的排放,常采用的措施是,将煤转化为清洁气体燃料。
已知:
2H2(g)+ O2(g)=2H2O(g) △H=-483.6kJ/mol
2C(s) + O2(g)=2CO(g) △H=-221kJ/mol
请写出焦炭与水蒸气反应的热化学方程式________________。
(4)根据(2)中汽车尾气净化原理,若该反应为放热反应,且该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应进行到t1时刻时达到平衡状态的是____。(填序号,下图中的v正、K、n、W分别表示正反应速率、平衡常数、物质的量、质量分数。)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一盛有饱和Na2CO3溶液的烧杯中插入惰性电极,保持温度不变,通电一段时间后:
A. 溶液的碱性增强; B. 溶液的浓度不变,有晶体析出;
C. 溶液的浓度增大; D. Na+和CO32-的浓度减小;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com