
【题目】在科学史上每一次重大的发现都极大地推进了科学的发展。下列对化学史的描述正确的是
A. 侯德榜制的碱是NaOH B. 阿伏加德罗提出分子的概念
C. 道尔顿发现电子 D. 凯库勒的贡献在于制备氯气
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】菲索菲那定(E)可用于减轻季节性过敏鼻炎引起的症状,其合成路线如下(其中R—为![]() ):
):

(1)A的名称是_______。C中含氧官能团的名称是_______。
(2)D的结构简式是_______。
(3)流程图中属于取代反应的是_______(填数字编号)。
(4)反应②的化学方程式是_______。
(5)G是B的同系物,分子式为C8H8O2,G的结构有_______种。其中,核磁共振氢谱吸收峰面积之比为1:2:2:2:1的结构简式是_______。
(6)已知: ,请以丙酮(CH3COCH3)、乙醇为原料制备A,写出相应的合成路线流程图(无机试剂任选)_______。
,请以丙酮(CH3COCH3)、乙醇为原料制备A,写出相应的合成路线流程图(无机试剂任选)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,可能共存的是( )
A.NH4+、CO32﹣、K+、Na+
B.Na+、Ba2+、Cl﹣、HCO3﹣
C.NO3﹣、Cu2+、K+、SO42﹣
D.K+ , Na+ , Cl﹣ , NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.同温同压下,相同体积的物质,其物质的量一定相等
B.任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等
C.1L一氧化碳气体一定比1L氧气的质量小
D.相同条件下的一氧化碳气体和氮气,若物质的量相等则体积相等,但质量不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组设计如下实验装置(图中夹持装置省略)测定制备的CaCO3粉末的纯度(样品中杂质不与酸反应,反应前装置中的CO2已全部排出)。下列说法错误的是
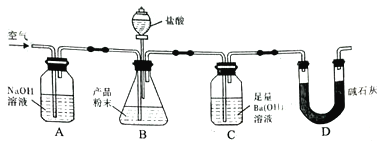
A. 缓入空气的作用是将反应结束后装置中残留的CO2全部鼓入到C装置中被吸收
B. A装置和D装置都是为了防止空气中的CO2气体进入C 装置而产生误差
C. 为了防止B 中盐酸挥发产生干扰,必须在B、C装置中间加一个装有饱和碳酸氢钠溶液的洗气瓶
D. 若CaCO3样品的质量为x,从C 中取出的沉淀洗净干燥后的质量为y,则CaCO3的纯度为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 0.1 mol·L-1的Na2CO3溶液中:c(OH-)=c(HCO![]() )+c(H+)+c(H2CO3)
)+c(H+)+c(H2CO3)
B. 25 ℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH
C. 常温下将10mlpH=4的醋酸溶液稀释至100ml,所得溶液4<pH<5
D. 向NaAlO2溶液中滴加NaHCO3溶液相互促进水解,有沉淀和气体生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图所示装置,在平底烧瓶的底部有一块钠,平底烧瓶内是干燥的空气。

过一段时间后可观察到______________,发生反应的化学方程式为___________________。
(2)某班同学用如图所示装置测定空气里氧气的含量。先用弹簧夹夹住橡胶管。点燃钠,伸入瓶中并塞上瓶塞。待钠熄灭并冷却后,打开弹簧夹,观察广口瓶内水面的变化情况。

①上述实验过程中发生反应的化学方程式为____________________________________。
②实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5,乙同学的广口瓶内水面上升明显大于瓶内空气体积的1/5。下列对这两种现象解释合理的是________。
a.甲同学可能使用钠的量不足,瓶内氧气没有消耗完
b.甲同学可能未塞紧瓶塞,钠熄灭冷却时外界空气进入瓶内
c.乙同学可能没夹紧弹簧夹,钠燃烧时瓶内部分空气受热从导管逸出
d.乙同学可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N、Cu、H、O、S、Mg是常见的六种元素。
(1)Mg位于元素周期表第______周期第______族;N与O的基态原子核外未成对电子个数比为_______;Cu的基态原子电子排布式为______。
(2)用“>”或“<”填空:
碱性:Mg(OH)2______Cu(OH)2 第一电离能:O______N
熔点:MgS______MgO 稳定性:H2S______H2O
(3)Mg在空气中燃烧可微量生产氮化镁(Mg3N2),Mg3N2(S)溶于足量的稀硫酸可得到两种正盐,在25℃、101kPa下,已知该反应每消耗1molH2SO4放热akJ,则该反应的热化学方程式为______。
(4)工业上采取加热条件下用氨气还原氧化铜制取铜,同时得到两种无污染的气体(或蒸汽),写出该反应的化学方程式,并标出电子转移的方向和数目______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com