
下列说法正确的是
A.常温下,pH = 7的氨水与氯化铵的混合溶液中:c(Cl-) = c(NH4+)
B.常温下pH = 5的盐酸溶液稀释1000倍后pH = 8
C.在BaSO4的饱和溶液中加入一定量Na2SO4固体,BaSO4的溶解度和Ksp均变小
D.0.1 mol·L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)
AD
【解析】
试题分析:氨水与氯化铵的混合溶液中存在的四种离子是NH4+、H+、OH-、Cl-,根据电中性可得:c(H+)+c(NH4+)=c(Cl-)+c(OH-),混合溶液pH=7说明c(H+)=c(OH-),则c(NH4+)=c(Cl-),故A正确;盐酸显酸性,无论怎样稀释,稀释后溶液仍显酸性,pH只能无限地接近7,不可能大于等于7,故B错误;加入硫酸钠固体,增大硫酸根离子浓度,使BaSO4(s) 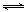 Ba2++SO42-的平衡向逆反应方向移动,析出沉淀导致硫酸钡的溶解度减小,说明硫酸钡在水中的溶解度比在硫酸钠溶液中的溶解度大,但是Ksp只与温度有关,温度不变溶度积不变,故C错误;硫酸铵是强电解质,则(NH4)2SO4=2NH4++SO42-,不考虑水解时,铵根离子的浓度是硫酸根离子浓度的2倍,硫酸根离子不能水解,少部分铵根离子水解,导致溶液呈弱酸性,大部分铵根离子不水解,则溶液中铵根浓度介于硫酸根离子浓度的1~2倍之间,所以稀硫酸铵溶液中c(NH4+)>c(SO42-)>c(H+)>c(OH-),故D正确。
Ba2++SO42-的平衡向逆反应方向移动,析出沉淀导致硫酸钡的溶解度减小,说明硫酸钡在水中的溶解度比在硫酸钠溶液中的溶解度大,但是Ksp只与温度有关,温度不变溶度积不变,故C错误;硫酸铵是强电解质,则(NH4)2SO4=2NH4++SO42-,不考虑水解时,铵根离子的浓度是硫酸根离子浓度的2倍,硫酸根离子不能水解,少部分铵根离子水解,导致溶液呈弱酸性,大部分铵根离子不水解,则溶液中铵根浓度介于硫酸根离子浓度的1~2倍之间,所以稀硫酸铵溶液中c(NH4+)>c(SO42-)>c(H+)>c(OH-),故D正确。
考点:考查溶液的pH和离子浓度大小关系,涉及电荷守恒原理、强酸无限稀释前后的pH、沉淀溶解平衡的移动与溶度积的关系、弱电解质、强电解质、盐类水解等。


科目:高中化学 来源: 题型:阅读理解

| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol CH3OCH3、1mol H2O | 2mol CH3OH | 1mol CH3OH |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 吸收a kJ | 放出b kJ | 放出c kJ |
| 平衡时体积(L) | V1 | V2 | V3 |
| 反应物转化率 | α 1 | α 2 | α 3 |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 非金属元素氮有多种氧化物,如NO、NO2、N2O4等.
非金属元素氮有多种氧化物,如NO、NO2、N2O4等.| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
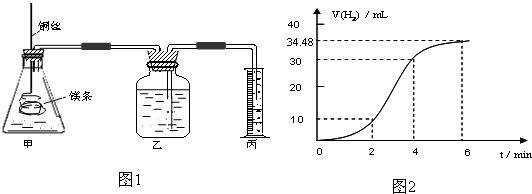
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
| 20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
| 水的体积/mL | 15 | 14.5 | V4 | 13.5 |
| 所需时间t/s | t1 | t2 | t3 | t4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com