
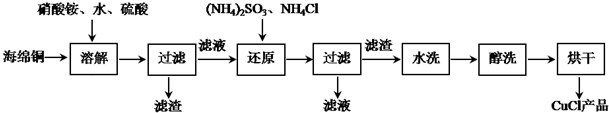
���� ��1����Ӧ�����Һ�в������������ӣ�˵��������Ӧ�У��������������ӷ�Ӧ���������Ӻ�ˮ��������������Ӧ�����������ӣ����������ӷ�Ӧ�����������ݴ�д����Ӧ�����ӷ���ʽ��
��2��������������������ʵ���������������ϵ�������غ���ʽ��������ߵ����ʵ������ټ�����������ɣ�
��3�����ݷ�Ӧ�����������Ϊ�����֣�һ������������������Ӧ����һ����ʣ������Һ�У����ݷ�Ӧ�����ɲ���Ϊ���������������Ӧ���ĵ����ᣬ��ۡ����������ʵ����������$\frac{3}{5}$�������ԭ��Һ�������Ũ�ȣ�
��� �⣺��1����ϡ����������������������Ļ�����У���Ӧ�����Һ�в������������ӣ�������Ӧ�У�Fe2O3+6H+=2Fe3++3H2O��Fe+2Fe3+=3Fe2+��Fe+2H+=Fe2++H2����
�ʴ�Ϊ��Fe2O3+6H+=2Fe3++3H2O��Fe+2Fe3+=3Fe2+��Fe+2H+=Fe2++H2����
��2����Ӧ����������ʣ�࣬˵��������������ȫ��Ӧ�����������ʵ���Ϊx�������������ʵ���Ϊy�����������ɵã���56x+160y=19.2��
���ɵı����3.36L���������ʵ���Ϊ��$\frac{3.36L}{22.4L/mol}$=0.15mol������0.15mol�����õ�0.15mol��2=0.3mol���ӣ�ymol������ת�����������ӵõ�2ymol���ӣ�xmol��ʧȥ2xmol���ӣ����ݵ���غ�ɵã���2y+0.3=2x��
���ݢ٢���ɷ������ã�x=0.2��y=0.05��
���Ի��������������Ϊ��56g/mol��0.2mol=11.2g��������������Ϊ��160g/nol��0.05mol=8g��
�𣺻������������������������Ϊ 11.2g��8g��
��3��������������������ȫ��Ӧ������FeSO4������ԭ���غ㣬�����������ܹ����ĵ���������ʵ���Ϊ��n��H2SO4��=n��Fe��+2n��Fe2O3��=0.2mol+0.05mol��2=0.3mol�����뷴Ӧ����������ʵ���Ũ��Ϊ��c��H2SO4��=$\frac{0.3mol}{0.25L}$=1.2mol/L��
���������ʵ����������$\frac{3}{5}$��������Һ������䣬�����ĵ���������ʵ���Ũ��Ϊԭ��Һ������Ũ�ȵ�$\frac{3}{5}$��
����ԭ��Һ�������Ũ��Ϊ��c��H2SO4��=$\frac{1.2mol/L}{\frac{3}{5}}$=2mol/L��
������ϡ��������ʵ���Ũ����2 mol/L��
���� ���⿼�����йػ����ļ��㣬��Ŀ�Ѷ��еȣ���ȷ��Ӧʵ�ʡ���Ӧ���Ⱥ�˳���ǽ���ؼ���ע�������غ㡢ԭ���غ��ڼ������Ӧ�÷���������������ѧ���ķ�����������ѧ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 18O��31P��119Sn | B�� | 27Al��19F��12C | ||
| C�� | 7N��15P��33As��51Sb��83Bi | D�� | ֻ��һ�����Ӳ��ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��ϵͳ������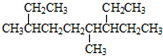 ������Ϊ��4��7-����-3-�һ����� ������Ϊ��4��7-����-3-�һ����� | |
| B�� | �����ʵ�����Na��NaOH��NaHCO3�ֱ����������л��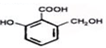 ����ַ�Ӧ�����ĸ��л�������ʵ���֮��Ϊ2��3��6����֪���Դ�С��ϵ ����ַ�Ӧ�����ĸ��л�������ʵ���֮��Ϊ2��3��6����֪���Դ�С��ϵ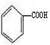 ��H2CO3�� ��H2CO3�� �� �� | |
| C�� | �Ҵ��Ͷ����ѻ�Ϊͬ���칹�壬CH3-CH=CH-CH3��C3H6һ����Ϊͬϵ�� | |
| D�� | �����ʡ���֬���Ǿ�����һ��������ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��� | �� | �� | �� |
| �� | CO2 | SO2 | ʯ��ˮ |
| �� | HCl | CO2 | ʯ��ˮ |
| �� | CO2 | SO2 | Ba��NO3��2 |
| �� | NO2 | SO2 | BaCl2 |
| �� | CO2 | NH3 | CaCl2 |
| A�� | �ڢۢ� | B�� | �٢ۢ� | C�� | �٢ڢۢ� | D�� | �٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ը��������Һ�����������ϩ | |
| B�� | ��BaCl2��ȥNaOH ��Һ�л��е�����Na2SO4 | |
| C�� | ��KSCN��Һ������Һ�к��е�Fe2+ | |
| D�� | ���ܽ⡢���˵ķ�������CaCl2��NaCl�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ�� | B�� | ��ˮ�� | C�� | ���� | D�� | ���ӷ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
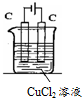 ����Ȼ�ͭ��Һ�Ļ�ѧ����ʽΪCuCl2$\frac{\underline{\;ͨ��\;}}{\;}$Cu+Cl2�����������У�Cu2+�����������ƶ���Cl-������ʧ���ӣ�����������Ӧ�����������ԭ�������������У������0.4mol�ĵ��ӷ���ת�ƣ�����������������������12.8g��
����Ȼ�ͭ��Һ�Ļ�ѧ����ʽΪCuCl2$\frac{\underline{\;ͨ��\;}}{\;}$Cu+Cl2�����������У�Cu2+�����������ƶ���Cl-������ʧ���ӣ�����������Ӧ�����������ԭ�������������У������0.4mol�ĵ��ӷ���ת�ƣ�����������������������12.8g���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com