
 ͼ�У�PΪһ�����ɻ����Ļ������ر�K���ֱ�������A��B�и�����2molX��2molY����ʼʱ��VA=aL��VB=0.8aL����ͨ�ܵ�������Բ��ƣ�������ͬ�¶Ⱥ��д������ڵ������£��������и��Է���������Ӧ��
ͼ�У�PΪһ�����ɻ����Ļ������ر�K���ֱ�������A��B�и�����2molX��2molY����ʼʱ��VA=aL��VB=0.8aL����ͨ�ܵ�������Բ��ƣ�������ͬ�¶Ⱥ��д������ڵ������£��������и��Է���������Ӧ������ ��1����ʼʱA����������A��ѹǿС������ӦΪ�������ʵ�����С�ķ�Ӧ��AΪ���º��ݣ�ƽ���ѹǿ��С��BΪ���º�ѹ����ЧΪ��Aƽ��Ļ���������ѹǿ����A��ƽ����ȣ�ƽ�������ƶ�����ƽ��ʱB��������������ʵ�����A�е�С��������������������䣬�ٸ���M=$\frac{m}{n}$�жϣ�
��2����������ܶ�=������������������ݻ��������ݻ���֪����Ҫ����������������������������������ʼʱX��Y����֮�ͣ�Ҳ���Ե�ЧΪ��ʼ����$\frac{4}{3}$molZ��$\frac{4}{3}$molW�����ƽ�⣬�������������������ʼʱZ��W����֮�ͣ�
��3����K��һ��ʱ���Ӧ�ٴδﵽƽ�⣬��ЧΪ��ʼ����4molX��4molY�����ƽ�⣬���º�ѹ����B��ƽ��Ϊ��Чƽ�⣬��Ӧ��ת���ʲ��䣬ƽ��ʱ������������ʵ���ΪB��2�������º�ѹ��ѹǿ֮�ȵ������ʵ���֮�ȣ��������㿪ʼ����4molX��4molY�����ƽ��ʱ���������ȥ����A�������ΪB���������
��� �⣺��1����ʼʱA����������A��ѹǿС������ӦΪ�������ʵ�����С�ķ�Ӧ��AΪ���º��ݣ�ƽ���ѹǿ��С��BΪ���º�ѹ����ЧΪ��Aƽ��Ļ���������ѹǿ����A��ƽ����ȣ�ƽ�������ƶ�����ƽ��ʱB��������������ʵ�����A�е�С��������������������䣬�ٸ���M=$\frac{m}{n}$��֪��MA��MB��
�ʴ�Ϊ������
��2����������ܶ�=������������������ݻ��������ݻ���֪����Ҫ����������������������������������ʼʱX��Y����֮�ͣ�Ҳ���Ե�ЧΪ��ʼ����$\frac{4}{3}$molZ��$\frac{4}{3}$molW�����ƽ�⣬�������������������ʼʱZ��W����֮�ͣ�����Ҫ���ٻ���Ҫ֪���������ǣ�X��YĦ��������Z��WĦ��������
��ѡ��A��B��
��3����K��һ��ʱ���Ӧ�ٴδﵽƽ�⣬��ЧΪ��ʼ����4molX��4molY�����ƽ�⣬���º�ѹ����B��ƽ��Ϊ��Чƽ�⣬��Ӧ��ת���ʲ��䣬ƽ��ʱ������������ʵ���ΪB��2�������º�ѹ��ѹǿ֮�ȵ������ʵ���֮�ȣ���ʼ����4molX��4molY�����ƽ��ʱ�����Ϊ0.6aL��2=1.2aL����B�������Ϊ1.2aL-aL=0.2aL��
�ʴ�Ϊ��0.2a��
���� ���⿼�黯ѧƽ����㣬�漰��Чƽ�����⣬�ϺõĿ���ѧ��������������������ؼ��ǵ�Чƽ��;���Ľ������Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | MgSO4 ��Һ��Ba��OH��2��Һ��Ӧ��SO42-+Ba2+�TBa SO4�� | |
| B�� | ����ˮ�ķ�Ӧ��2Na+2H2O�T2Na++2OH-+H2�� | |
| C�� | ��Ƭ������������Һ��Ӧ��2Al+2OH--+2H2O�TAlO2-+3H2�� | |
| D�� | �������������������Fe��OH��3+3H+�TFe3++3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t/s | 0 | 50 | 100 |
| c��N2O5��/mol•L-1 | 5.0 | 3.5 | 2.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
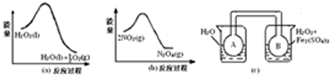
 ������Ԫ��X��Y��Z��������Ϊ1��7��12�γɵĻ����������������ӵ����ӷ�Ӧ����ʽ�ǣ�
������Ԫ��X��Y��Z��������Ϊ1��7��12�γɵĻ����������������ӵ����ӷ�Ӧ����ʽ�ǣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com