
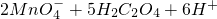 ═
═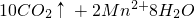 ,下列分析错误的是
,下列分析错误的是


科目:高中化学 来源: 题型:阅读理解
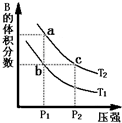 对于反应A(g)?2B(g)△H>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示.回答下列各题.
对于反应A(g)?2B(g)△H>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示.回答下列各题.| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(B)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(A)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 对于可逆反应:2A(g)+B(g)?2C(g),分别测定反应在不同温度下达到平衡时B的转化率,绘制了如图所示的曲线,图中a、b、c三点分别表示不同的时刻状态.下列分析正确的是( )
对于可逆反应:2A(g)+B(g)?2C(g),分别测定反应在不同温度下达到平衡时B的转化率,绘制了如图所示的曲线,图中a、b、c三点分别表示不同的时刻状态.下列分析正确的是( )| A、该反应的△H<0 | B、b点时混合气体的平均摩尔质量不再变化 | C、增大压强,可使a点达到T1温度下平衡状态 | D、c点表示的状态:v(正)<v(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇.
乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇.| 催化剂 |
| 催化剂 |
 |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com