
����Ŀ����ͼ��ֱ��Ǽס�������ͬѧ����Ӧ��AsO ![]() +2I��+2H+AsO
+2I��+2H+AsO ![]() +I2+H2O����Ƴɵ�ԭ���װ�ã�����C1��C2��Ϊ̼����������ͼ���ձ�����μ�������Ũ���������ͼ��B�ձ�����μ�������40%NaOH��Һ��������������ȷ���ǣ� ��
+I2+H2O����Ƴɵ�ԭ���װ�ã�����C1��C2��Ϊ̼����������ͼ���ձ�����μ�������Ũ���������ͼ��B�ձ�����μ�������40%NaOH��Һ��������������ȷ���ǣ� �� 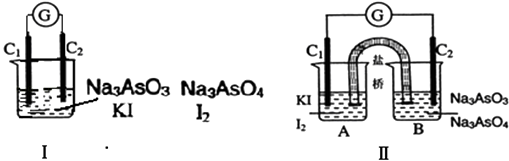
A.�������ʱ������
B.ָ�뷢��ƫת
C.�������ʱ����Һ��ɫ����
D.�������ʱ��C2������
E.�������ʱ��C1�Ϸ����ĵ缫��ӦΪI2+2e���T2I��
���𰸡�BD
���������⣺A���������ʱ�������缫��Ϊ̼����������ԭ��ط�Ӧ����������G��ָ�벻����ƫת����A����B��������Ӧ���ɵⵥ�ʣ�����Һ��ɫ�����B��ȷ��
C���������ʱ��C2����������AsԪ��ʧȥ���ӣ���C����
D���������ʱ��C1�ϵõ����ӣ�Ϊ�����������ĵ缫��ӦΪI2+2e���T2I�� �� ��D��ȷ��
��ѡBD��
������ͼ���ձ�����μ�������Ũ���ᣬ����������ԭ��Ӧ��������ԭ��ط�Ӧ���Դ˷���A��B��
������ͼ��B�ձ�����μ�������40%NaOH��Һ����������ѧ��Ӧ������ԭ��ط�Ӧ��A�з���I2+2e���T2I�� �� Ϊ������Ӧ����B��As���ϼ����ߣ�����������Ӧ���Դ˷���C��D��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ȤС���ijƷ��������Ħ�����ɷּ��京����������̽����������ϣ�������Ħ������̼��ơ�����������ɣ������������ɷ���������ʱ���������ɣ�
��1����Ħ���������������Ķ��Լ���ȡ����������Ʒ����ˮ�ɷֽ��衢���ˣ�
���������м������NaOH��Һ�����ˣ�����������NaOH��Һ��Ӧ�����ӷ���ʽ�� ��
������������Һ����ͨ�����������̼���ټ������ϡ���ᣮ�۲쵽�������� ��
��2����������Ʒ��̼��ƵĶ����ⶨ������ͼ��ʾװ�ã�ͼ�мг�������ȥ������ʵ�飬��ַ�Ӧ�ⶨC�����ɵ�BaCO3������������ȷ��̼��Ƶ�����������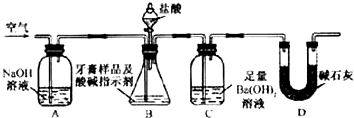
����ʵ����̻ش��������⣺
��ʵ����������������ͨ������������ó��˿ɽ���B��C�еķ�Ӧ���⣬���У� ��
��C�з�Ӧ����BaCO3�Ļ�ѧ����ʽ�� ��
�����и����ʩ�У�������߲ⶨȷ�ȵ��������ţ���
a���ڼ�������֮ǰ��Ӧ�ž�װ���ڵ�CO2����
b���μ�����˹���
c����A��B֮������ʢ��Ũ�����ϴ��װ��
d����B��C֮������ʢ�б���̼��������Һ��ϴ��װ��
��ʵ����ȷ��ȡ8.00g��Ʒ���ݣ��������βⶨ�����BaCO3ƽ������Ϊ3.94g������Ʒ��̼��Ƶ���������Ϊ ��
��������Ϊ���زⶨC�����ɵ�BaCO3������ֻҪ�ⶨװ��C������CO2ǰ��������һ������ȷ��̼��Ƶ�����������ʵ��֤�����˷����ⶨ�Ľ������ƫ�ߣ�ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ԫ���й�������������߱��������Ӧ�ո���:
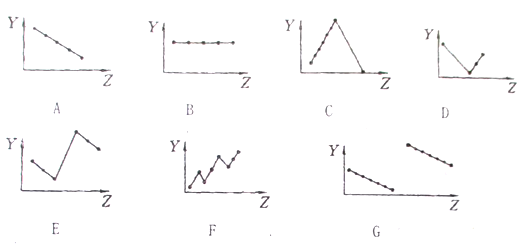
��1����IIA��Ԫ�صļ۵�����_________��
��2����������Ԫ�ص�����ϼ���_______ ��
��3������������۵�_______ ��
��4��������������Na+��Mg2+��A13+��P3-��S2-��Cl-�����Ӱ뾶_______ ��
��5���ڶ���������Ԫ����ԭ����������ԭ�Ӱ뾶�ı仯_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������е����ɵ��Ӹ����ڷ��ӻ�ԭ�����γɵĿ���������(Ҳ��������)����Ϊ������ά���ء���O22-����һ�ֿ��������ӣ���Ħ������Ϊ�� ��
A. 32gB. 34gC. 32g��mol��1D. 34g��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǿ�����ˮ�������ʾ��ˮ��̶ȵĴ�С����������ˮ������ʵ���ռԭ���ܵĵ�������ʵ����ķ�������ʾ�ģ������2L 0.1mol/L��ǿ��������NaA��Һ�ij����µ�pHΪ10����A����ˮ���Ϊ�� ��
A.0.01%
B.0.1%
C.0.2%
D.1%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣���Ԣ١���Ԫ���ڱ��е�λ�ã��ش��������⣺
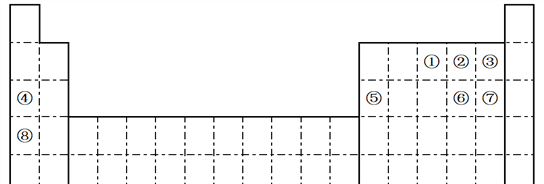
��1����Ԫ����Ԫ�����ڱ��е�λ��Ϊ________________________��
��2��д���ں���10�����ӵĺ��صĻ�ѧ����______________��
��3���ڢ�����������������Ԫ���У������Ӱ뾶���ɴ�С������˳��Ϊ_______________________________________________���������ӷ��űȽϴ�С��
��4������������Ԫ���������⻯����ȶ�����ǿ������˳����_______________________________________________�����û�ѧʽ�Ƚ�ǿ����
��5����д���ٵ��⻯����������Ļ�ѧ����ʽ______________________________��
��6���ɢڢܢ�����Ԫ����ɵ�һ�����ڿ����з��û���ʣ����û�ѧ����ʽ��ʾ���ʵķ�Ӧ_______________________________________________��
��7���ڢ���ߵĵ����У���ѧ���ʽϻ��õ���___________���ѧʽ����������������ʵ֤���������۵���_____________��
a��Ԫ�آ��ʵ��۵��Ԫ�آߵ��ʵ��۵��
b��Ԫ�آߵ��⻯���Ԫ�آ��⻯���ȶ�
c��Ԫ�آߵ��⻯���ˮ��Һ������ǿ��Ԫ�آ��⻯���ˮ��Һ������
d��һ�������¢͢ߵĵ��ʷֱ���Cu��Ӧʱ���߲����е�ͭԪ�ؼ�̬����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣���Ա��еĢ١�����Ԫ�أ���Ԫ�ط��Ż�ѧʽ��ջش��������⣺
���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
�� | �� | �� | ||||||
�� | �� | �� | �� | �� | �� | �� | ||
�� | �� | �� |
(1)�ڢۡ���Ԫ���У�ԭ�Ӱ뾶������___________�������ӵ�ԭ�ӽṹʾ��ͼΪ___________
(2)�١���Ԫ���У�����������Ӧ��ˮ������������ǿ����________��������ǿ����________�������Ե�����������________���������Ӧ�����ӷ���Ϊ__________��__________��__________��
(3)Ԫ�آڵ�һ��ԭ������������������1����m�˴���ԭ���γɵļ������к��еĵ�����Ϊ______________mol��
(4)�ڢ����ĵ����У���ѧ���ʽϻ��õ���___________������ʲô��ѧ��Ӧ˵������ʵ(д����Ӧ�Ļ�ѧ����ʽ)��___________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CH3COOHΪ���������ᣬ�ڹ�ҵ�������������й㷺��Ӧ�ã�
��1���������к�100mL pH=3��CH3COOH��Һ��1L pH=4��CH3COOH��Һ����Ҫ�����ʵ���Ũ�ȵ�NaOH��Һ������ֱ�ΪV1��V2 �� ��V1V2 �����������=�����������кͺ�������Һ������Ũ���ɴ�С��˳��Ϊ ��
��2����0.1000molL��1NaOH��Һ�ζ�20.00mLijδ֪Ũ�ȵĴ�����Һ���ζ�������ͼ��ʾ��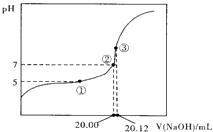
���Тٵ���ʾ��Һ��c��CH3COO����=2c��CH3COOH����
�۵���ʾ��Һ�д��ڣ�c��CH3COO����+c��CH3COOH���Tc��Na+������CH3COOH�ĵ���ƽ�ⳣ��Ka= �� CH3COOH��ʵ��Ũ��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵķ�������������
A. ������������������ʯ��B. ������ռ����þ������
C. �Σ�ʳ�Ρ�ʯ��ʯ����ʯ��D. ���ʣ�ʯī��������ˮ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com