
 ЃЉЪЧвЛжжЙуЦзадЕФжївЊгУгквЖУцБЃЛЄЕФЩБОњМСЃЌЮовЉКІЃЌдкЙћЪїЁЂЪпВЫМАИїжжОМУзїЮяЩЯЪЙгУЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
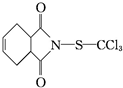
ЃЉЪЧвЛжжЙуЦзадЕФжївЊгУгквЖУцБЃЛЄЕФЩБОњМСЃЌЮовЉКІЃЌдкЙћЪїЁЂЪпВЫМАИїжжОМУзїЮяЩЯЪЙгУЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ| AЃЎ | ПЫОњЕЄЕФЗжзгЪНЮЊC9H8O2NSCl3ЃЌЪєгкЗМЯузхЛЏКЯЮя | |
| BЃЎ | ПЫОњЕЄвзШмгкЫЎЃЌдкМгШШЬѕМўЯТВЛФмгыNaOHШмвКЗДгІ | |
| CЃЎ | ПЫОњЕЄФмгыфхЕФCCl4ШмвКЗЂЩњШЁДњЗДгІЪЙжЎЭЪЩЋ | |
| DЃЎ | ПЫОњЕЄдквЛЖЈЬѕМўЯТФмЗЂЩњШЁДњЁЂМгОлЕШЗДгІ |
ЗжЮі гЩНсЙЙПЩжЊЃЌЗжзгжаКЌЬМЬМЫЋМќЁЂєЪЛљЁЂ-ClЃЌНсКЯЯЉЬўЁЂЭЊЁЂТБДњЬўЕФаджЪРДНтД№ЃЎ
НтД№ НтЃКAЃЎПЫОњЕЄЗжзгжаВЛКЌБНЛЗЃЌВЛЪєгкЗМЯузхЛЏКЯЮяЃЌЙЪAДэЮѓЃЛ
BЃЎПЫОњЕЄВЛвзШмгкЫЎЃЌдкМгШШЬѕМўЯТЃЌТШдзгФмгыNaOHШмвКЗЂЩњЫЎНтЗДгІЃЌЙЪBДэЮѓЃЛ
CЃЎКЌЬМЬМЫЋМќЃЌФмгыфхЕФCCl4ШмвКЗЂЩњМгГЩЗДгІЃЌЙЪCДэЮѓЃЛ
DЃЎКЌЬМЬМЫЋМќПЩЗЂЩњМгОлЗДгІЃЌКЌ-ClПЩЗЂЩњШЁДњЗДгІЃЌЙЪDе§ШЗЃЛ
ЙЪбЁDЃЎ
ЕуЦР БОЬтПМВщгаЛњЮяЕФНсЙЙгыаджЪЃЌЮЊИпЦЕПМЕуЃЌАбЮеЙйФмЭХгыаджЪЕФЙиЯЕЮЊНтД№ЕФЙиМќЃЌВржиЗжЮігыгІгУФмСІЕФПМВщЃЌзЂвтЯЉЬўЁЂТБДњЬўЕФаджЪЃЌЬтФПФбЖШВЛДѓЃЎ


 УћаЃУћЪІХргХзївЕБОМгКЫаФЪдОэЯЕСаД№АИ
УћаЃУћЪІХргХзївЕБОМгКЫаФЪдОэЯЕСаД№АИ ШЋГЬН№ОэЯЕСаД№АИ
ШЋГЬН№ОэЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКНтД№Ьт
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКНтД№Ьт

ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКбЁдёЬт
| AЃЎ | ЭЈЙ§ЛЏбЇБфЛЏвЛЖЈФмИФБфЮяжЪЕФаджЪ | |
| BЃЎ | ШЫУЧЫљЪЙгУЕФВФСЯЃЌЖМЪЧДПЖШдНИпдНКУ | |
| CЃЎ | бѕЛЏЛЙдЗДгІжавЛЖЈЛсЗЂЩњЕчзгзЊвЦ | |
| DЃЎ | ФГдЊЫигЩЛЏКЯЬЌБфЮЊгЮРыЬЌЃЌИУдЊЫигаПЩФмБЛбѕЛЏЃЌвВгаПЩФмБЛЛЙд |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКНтД№Ьт
 ЮЊНтОіФмдДЖЬШБЮЪЬтЃЌЙЄвЕЩњВњжагІКЯРэРћгУЛЏбЇФмЃЎ
ЮЊНтОіФмдДЖЬШБЮЪЬтЃЌЙЄвЕЩњВњжагІКЯРэРћгУЛЏбЇФмЃЎ| ЛЏбЇМќ | H-H | N-H | NЁдN |
| МќФм/kJ•mol-1 | 436 | a | 945 |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКЖрбЁЬт
 ЃЌПЩгУзїПЙФ§бЊвЉЃЎЯТСаЙигкЫЋЯуЖЙЫиЕФЭЦТлжаДэЮѓЕФЪЧЃЈЁЁЁЁЃЉ
ЃЌПЩгУзїПЙФ§бЊвЉЃЎЯТСаЙигкЫЋЯуЖЙЫиЕФЭЦТлжаДэЮѓЕФЪЧЃЈЁЁЁЁЃЉ| AЃЎ | ЗжзгЪНЮЊC19H14O6ЃЌФмгыNaOHШмвКЗДгІ | |
| BЃЎ | ЪГВнЖЏЮяЪГгУИЏАмВнСЯКѓЃЌдкЪмЭтЩЫЪБбЊвКВЛШнвзФ§ЙЬ | |
| CЃЎ | ЗжзгжаЫљгаЬМдзгВЛПЩФмдкЭЌвЛЦНУц | |
| DЃЎ | ПЩЗЂЩњЫЎНтЁЂМгГЩЁЂбѕЛЏЁЂЛЙдЗДгІ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКбЁдёЬт
| AЃЎ | ГЃЮТГЃбЙЯТЃЌ20 g ФЪЦјЫљКЌгаЕФЗжзгЪ§ФПЮЊ0.5NA | |
| BЃЎ | ГЃЮТЯТЃЌ46 g ввДМКЌC-HМќЪ§ФПЮЊ6NA | |
| CЃЎ | 1.5 mol NO2гызуСПH2OЗДгІЃЌзЊвЦЕФЕчзгЪ§ЮЊNA | |
| DЃЎ | НЋ0.1 mol ввЫсввѕЅЕЮМгЕНЯЁСђЫсжаЫЎНтЃЌЩњГЩ0.1NAИіCH3COOHЗжзг |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКбЁдёЬт
 ГЃЮТЯТЃЌдк20mL0.1mol•L-1 H2RШмвКжаЕЮМг0.1mol•L-1 NaOHШмвКЃЌЛьКЯШмвКЕФpHгыЕЮМгЧтбѕЛЏФЦШмвКЬхЛ§ЃЈVЃЉЕФЙиЯЕШчЭМЫљЪОЃЎЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
ГЃЮТЯТЃЌдк20mL0.1mol•L-1 H2RШмвКжаЕЮМг0.1mol•L-1 NaOHШмвКЃЌЛьКЯШмвКЕФpHгыЕЮМгЧтбѕЛЏФЦШмвКЬхЛ§ЃЈVЃЉЕФЙиЯЕШчЭМЫљЪОЃЎЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ| AЃЎ | HR-ЕФЕчРыГЬЖШДѓгкЫЎНтГЬЖШ | |
| BЃЎ | ЂкЕуЖдгІШмвКжаРызгХЈЖШЕФЙиЯЕcЃЈNa+ЃЉЃМcЃЈH2RЃЉ+cЃЈHR-ЃЉ+cЃЈR2-ЃЉ | |
| CЃЎ | дкЂйЁЂЂкЁЂЂлЕуЖдгІЕФШмвКжаЃЌЫЎЕчРыЕФcЃЈH+ЃЉ•cЃЈOH-ЃЉзюДѓЕФЪЧЂл | |
| DЃЎ | ЕЮЖЈЧАЃЌШмвКжаДцдкСЃзгХЈЖШДѓаЁЙиЯЕЃКcЃЈH2RЃЉЃОcЃЈH+ЃЉЃОcЃЈHR-ЃЉЃОcЃЈR2-ЃЉЃОcЃЈOH-ЃЉ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃКНтД№Ьт
 ЃЈNH4ЃЉ2SO4•MnSO4•nH2OЃЈСђЫсУЬяЇЃЉЪЧЧГЗлЩЋОЇЬхЃЌвзШмгкЫЎЃЌдкХЉвЕЩЯгУзїЮЂСПдЊЫиЗЪСЯЃЌЪЕбщЪвгЩMnO2жЦБИСђЫсУЬяЇЕФЪЕбщВНжшШчЯТЃК
ЃЈNH4ЃЉ2SO4•MnSO4•nH2OЃЈСђЫсУЬяЇЃЉЪЧЧГЗлЩЋОЇЬхЃЌвзШмгкЫЎЃЌдкХЉвЕЩЯгУзїЮЂСПдЊЫиЗЪСЯЃЌЪЕбщЪвгЩMnO2жЦБИСђЫсУЬяЇЕФЪЕбщВНжшШчЯТЃКВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com