
| A.0.1 mol/LCH3COOH溶液中:c(CH3COO-)+ c(CH3COOH)=0.1mol/L |
| B.NaHCO3溶液中: c(OH-) = c(H+) + c(H2CO3)-c(CO32-) |
| C.CH3COONa溶液中:c(Na+)> c(CH3COO-)> c(OH-)> c(H+) |
| D.Na2S溶液中:2 c(Na+)= c(S2-) + c(HS-)+ c(H2S) |


科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
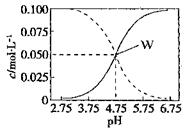
| A.pH=4的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| B.W点所表示的溶液中:c(Na+)+ c(H+)= c(CH3COOH)+c(OH-) |
| C.将W点所表示的1.0L溶液稀释到10L,用pH计测量,溶液的pH应为5.75 |
| D.pH=5.5的溶液中:c(Na+)+ c(H+)- c(OH-)+c(CH3COOH)=0.1mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.往CH3COOH溶液中加水,c(OHˉ)和c(H+)均增大 |
| B.物质的量浓度均为0.1mol?Lˉ1的CH3COOH溶液和NaOH溶液等体积混合,c(Na+)>c(CH3COOˉ) |
| C.某浓度的氯化铵溶液中存在c(NH4+)>c(Clˉ)>c(H+)> c(OHˉ) |
| D.在pH=4的氯化铵溶液中c(H+)+ c(NH4+)=" c(Clˉ)+" c(OHˉ) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(H+)=c(CH3COO-)+c(OH-) |
| B.加水稀释到原体积的10倍后溶液pH变为4 |
| C.加入少量乙酸钠固体,溶液pH降低 |
| D.与等体积pH=11的NaOH溶液混合后所得溶液中c(Na+)=c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.HA为一元强酸 |
| B.MOH为一元弱碱 |
| C.N点水的电离程度小于K点水的电离程度 |
| D.K点对应的pH=10,则有c (MOH)+ c(OH-)-c (H+)=0.005mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.石油裂化得到气态烯烃 | B.石油裂解目的重油转化轻质油 |
| C.我国“西气东输”工程的气指甲烷 | D.水煤气是通过煤的液化得到的气体燃料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com