
【题目】十九大报告中指出:“建设美丽中国,为人民创造良好生产生活环境,为全球生态安全作出贡献。”下列行为一般不会引起环境污染的是
A.冬季燃煤供暖B.废电池深埋降解
C.利用风能、太阳能发电D.节日燃放烟花爆竹
科目:高中化学 来源: 题型:
【题目】科学家预言,未来理想的燃料是绿色植物,即将植物的秸秆(主要成分是纤维素)用适当的催化剂使之水解成葡萄糖,再将葡萄糖转化成乙醇(葡萄糖在酒化酶的作用下可转化成乙醇和二氧化碳),用作燃料。
(1)请写出将绿色植物的秸秆转化为乙醇两步反应的化学方程式。
(2)现有1620t含纤维素约为50%的秸秆,理论上可制得80%的酒精多少吨?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识回答下列问题
(1)以K、Na、H、O、S、N中任两种或三种元素组成合适物质,分别填在表中②、④、⑥后面。
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①H2SO4 ②_______ | ③NaOH ④_______ | ⑤Na2SO4 ⑥_______ | ⑦CO2 ⑧SO3 | ⑨NH3 |
(2)写出①与少量的③溶液反应的离子方程式__________________________。
(3)写出铁与①溶液反应的化学方程式________________________________。
(4)某同学欲用10mol·L-1浓硫酸配制480 mL 1 mol·L-1的稀硫酸。配制480mL 1mol·L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为_________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取少量干燥的氨气涉及下列装置中,其中正确的是( )
A.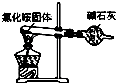
如图是氨气发生装置
B.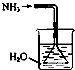
如图是氨气吸收装置
C.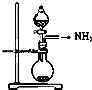
如图是氨气发生装置
D.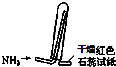
如图是氨气收集、检验装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】)硫酸钙来源于烟气脱硫、磷酸盐工业和其他工业的副产品,可用于生成硫酸及其硫化物等。硫酸钙在高温下被CO还原,发生的反应有:
I.CaSO4(s)+4CO(g) ![]() CaS(s)+4CO2(g) △Hl 平衡常数K1
CaS(s)+4CO2(g) △Hl 平衡常数K1
II.CaSO4(s)+CO(g) ![]() CaO(s)+SO2(g)+CO2(g) △H2 平衡常数K2
CaO(s)+SO2(g)+CO2(g) △H2 平衡常数K2
III.3CaSO4(s)+CaS(s) ![]() 4CaO(s)+4SO2(g) △H3=+1049.2kJ/mol 平衡常数K3
4CaO(s)+4SO2(g) △H3=+1049.2kJ/mol 平衡常数K3
(1)△H3=___(用△H1、△H2表示);平衡常数K3=_______(用K1、K2表示)。
(2)上述反应的平衡常数的对数值(lgK)与温度(T)的关系如下图所示:
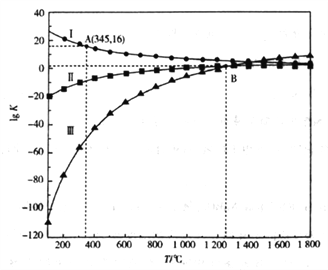
①△H1_________0(填”>”或”<")。
②若只发生反应I,A点c(CO)/c(CO2)=__________(填数值)。
③若只发生反应II和III,B点c(CO)、c(CO2)及c(SO2)之间的关系是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日前正在研发的两种由电化学制取氨的装置如图1和图2所示:

下列说法正确的是
A. 工作时,O2-向X极移动,H+向Z极移动
B. 两个电解池的电解总反应方程式完全相同
C. 两个电解池生成相同量NH3时,电路中流过电子的物质的量相同
D. 随着反应的进行,两种电解池中电解质不断减少,需及时补充电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4(草酸)是一种无色晶体,易溶于水,熔点为182℃,150~160℃升华,189.5℃分解。25℃时,Ka1=6×10-2,Ka2=6.4×10-5,Ksp(CaC2O4)=4.0×10-9。某校甲、乙、丙3个学习小组设计实验探究草酸的化学性质。
(1)草酸中所含官能团的名称为__________;
反应Ca2+(aq)+H2C2O4(aq)![]() CaC2O4(s)+2H+(aq),25℃时的平衡常数K=__________。
CaC2O4(s)+2H+(aq),25℃时的平衡常数K=__________。
(2)甲组同学在Na2CO3溶液中加入少量草酸溶液产生大量气体,他们查得H2CO3的Ka1=4.47×10-7,Ka2=4.68×10-11,则发生反应的离子方程式为______________。
(3)乙组同学在酸性KMnO4溶液中逐滴加入草酸溶液,溶液紫色逐渐褪去,说明草酸具有_____性,反应中氧化产物与还原产物的物质的量之比为_________。
(4)丙组同学设计下列装置分解H2C2O4并设计实验装置检验产物中的CO2和CO。
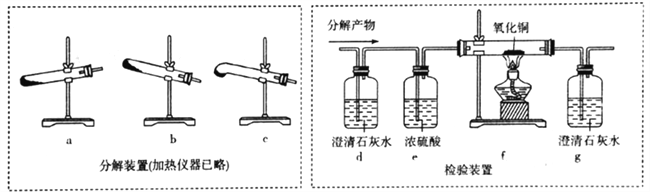 ①分解H2C2O4装置中最好的是__________(填字母)。
①分解H2C2O4装置中最好的是__________(填字母)。
②d中澄清石灰水变浑浊,能否说明有CO2生成? ___(填“能“或“不能”,下同),理由是________;仅依据装置g中澄清石灰水变浑浊,能否说明有CO生成?_________,理由是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有丰富的镁资源.某同学设计了从模拟海水中制备MgO的实验方案: 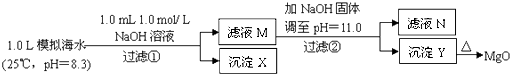
模拟海水中的 | Na+ | Mg2+ | Ca2+ | Cl﹣ | HCO3﹣ |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某种离子的浓度小于1.0×10﹣5 mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变.已知:Ksp(CaCO3)=4.96×10﹣9;Ksp(MgCO3)=6.82×10﹣6;Ksp[Ca(OH)2]=4.68×10﹣6;Ksp[Mg(OH)2]=5.61×10﹣12 . 下列说法正确的是( )
A.沉淀物X为CaCO3
B.滤液M中存在Mg2+ , 不存在Ca2+
C.滤液N中存在Mg2+、Ca2+
D.步骤②中若改为加入4.2gNaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( ) 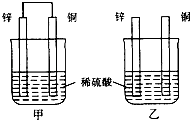
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均减小
D.产生气泡的速度甲比乙快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com