
【题目】下列操作或叙述正确的是( )
A.配制1mol?L﹣1NaOH溶液时,将溶解后的NaOH溶液立即注入容量瓶
B.用小刀切下一小块金属钠,将剩余的钠再放回原试剂瓶
C.向某溶液中加入BaCl2溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中一定含有 ![]()
D.向沸水中逐滴滴加1mol?L﹣1FeCl3溶液,并不断用玻璃棒搅拌,可制得Fe(OH)3胶体
【答案】B
【解析】解:A、NaOH固体溶于水放热,而容量瓶不能受热,故应将NaOH溶液冷却至室温再转移至容量瓶,故A错误;B、试验中剩余的液体药品和粉末状药品不能放回原试剂瓶,但块状的药品可以放回原试剂瓶,故B正确;
C、向某溶液中加入BaCl2溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中可能含有硫酸根离子,还可能是Ag+与BaCl2生成了AgCl,故C错误;
D、用玻璃棒搅拌胶体,可引起胶体的聚沉,故D错误.
故选B.
【考点精析】根据题目的已知条件,利用胶体的重要性质的相关知识可以得到问题的答案,需要掌握胶体的性质:①丁达尔现象(可用来鉴别胶体和溶液) ②布朗运动 ③电泳现象 ④胶体聚沉(加入电解质、加入带异种电荷的胶体、加热,均可使胶体聚沉).


科目:高中化学 来源: 题型:
【题目】用18mol/L 的浓硫酸配制 100mL 3.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③稀释 ④检漏、转移、洗涤 ⑤定容、摇匀 回答下列问题:
(1)所需浓硫酸的体积是mL,量取浓硫酸所用的量筒的规格是(用下列编号填空). A.10mL B.25mL C.50mL D.100mL
(2)第③步实验的具体操作是
(3)第⑤步实 验 的 操 作 是 继 续 向 容 量 瓶 中 注 入 蒸 馏 水 至 离 刻 度 线 , 改用向容量瓶中滴加蒸馏水至为止.塞紧瓶塞,倒转摇匀并装试剂瓶.
(4)下列情况对所配制的稀硫酸浓度有何影响?(填“偏大”“偏小”或“无影响”)①所用的浓硫酸长时间放置在密封不好的容器中;
②容量瓶用蒸馏水洗涤后残留有少量的水;
③在转入容量瓶前烧杯中溶液未冷却至室温;
④加水超过刻度线后,用胶头滴管吸出多余的液体 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下为从铝土矿(Al2O3、Fe2O3、泥沙)提取铝的流程图(注:整个流程中,不考虑泥沙的溶解及有关反应;C可以用来治疗胃酸过多):
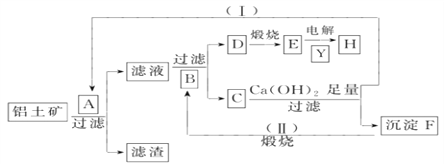
(1)A溶质的化学式___________;B的结构式____________,Y的名称_____________。
(2)写出①C与Ca(OH)2稀溶液反应的离子方程式: __________________________________。
②F→B的反应方程式: ______________________________。
(3)操作(Ⅰ)、(Ⅱ)在工业生产中的意义________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com