
【题目】如图是用0.1000mol/L的盐酸滴定某未知浓度的NaOH溶液的示意图和某次滴定前、后的盛放盐酸滴定管中液面的位置.请回答:
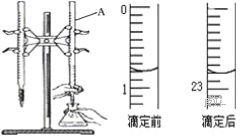
(1)仪器A的名称是__________________;
(2)盐酸的体积读数:滴定前读数为_____mL,滴定后读数为______mL;
(3)某实验小组同学的三次实验的实验数据如下表所示.根据表中数据计算出的待测NaOH溶液的浓度是________________;(保留四位有效数字)
实验 编号 | 待测NaOH溶液的体积(mL) | 滴定前盐酸的 体积读数mL) | 滴定后盐酸的 体积读数(mL) |
1 | 20.00 | 1.20 | 23.22 |
2 | 20.00 | 2.21 | 24.21 |
3 | 20.00 | 1.50 | 23.48 |
(4)滴定操作可分解为如下几步(所用的仪器刚用蒸馏水洗净):
A.用碱式滴定管向锥形瓶里注入20.00mL待测NaOH溶液,并加入2~3滴酚酞;
B.用标准溶液润洗酸式滴定管2~3次;
C.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液,使管内无气泡;
D.取标准盐酸注入酸式滴定管至刻度0以上2~3cm;
E.调节液面至0或0以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准盐酸滴定至终点并记下滴定管液面的刻度。
正确操作步骤的顺序是(用序号字母填写)_____________;
(5)判断到达滴定终点的实验现象是________________________________。
(6)对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
①如果上述B步骤省略,对测定结果的影响是_________;
②取待测液的滴定管,滴定前滴定管尖端有气泡,滴定后气泡消失._________;
③若滴定前锥形瓶未用待测液润洗,对测定结果的影响是___________;
④标准液读数时,若滴定前仰视,滴定后俯视,对测定结果的影响是___________.
【答案】 酸式滴定管 0.80 22.80 0.1100mol·L﹣1 BDCEAF 当溶液颜色由粉红色变为无色,且半分钟内不变色 偏高 偏低 无影响 偏低
【解析】(1)该滴定管的下端是玻璃活塞,所以仪器的名称为酸式滴定管;
(2)滴定前,滴定管中的液面读数为0.80mL,滴定后,滴定管中的液面读数为22.80mL;
(3)三次滴定消耗的体积为:22.02mL,22.00mL,21.98mL,数据均有效,则平均消耗
V(NaOH)=22.00mL,c(待测)=V(标准)×c(标准)/ V(待测)=
0.1000mol/L×22.00mL/20.00mL==0.1100 mol·L﹣1;
(4)中和滴定按照检漏、洗涤、润洗、装液、滴定等顺序操作,可知正确的操作顺序为:BDCEAF;
(5)滴定时,当溶液颜色由粉红色变为无色,且半分钟内不变色,可说明达到滴定终点;(6)①如果上述B步骤省略,即未用标准溶液润洗酸式滴定管2~3次,相当于标准液稀释,导致标准液的体积偏大,根据c(待测)= V(标准)×c(标准)/ V(待测)分析,C(待测)偏高;②取待测液的滴定管,滴定前滴定管尖端有气泡,滴定后气泡消失,待测液的物质的量偏小,导致标准液的体积偏小, C(待测)偏低;③若滴定前锥形瓶未用待测液润洗,待测液的物质的量不变,标准液的体积也不变,C(待测)不变;④标准液读数时,若滴定前仰视,滴定后俯视,导致标准液的体积偏小,C(待测)偏低。


科目:高中化学 来源: 题型:
【题目】“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中一种,若将纳米碳均匀地分散到
蒸馏水中,所形成的分散系:①是溶液②是胶体③能产生丁达尔效应④分散质粒子能透过滤纸⑤分散质粒子不能透过滤纸⑥静置后,会析出黑色沉淀.
A. ①④⑥ B. ②③④ C. ②③⑤ D. ①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在水溶液中能够大量共存的是
A. H+、SO42― 、 SO32― B. Ba2+、 CO32―、N O3―
C. Na+、Cl一、SO42― D. Ca2+、SO42―、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2A(g)+B(g)3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是( )
A.v(A)=0.7 mol/(L.min)
B.v(B)=0.3mol/(L.min)
C.v(C)=0.9 mol/(L.min)
D.v(D)=1.1mol/(L.min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒 。下列说法正确的是( )

A. 正极反应为AgCl+e-=Ag+Cl-
B. 电池工作时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用KCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.2 mol e-时,交换膜左侧溶液中约减少0.4 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是
A.具有相同通式的有机物不一定互为同系物
B.分子组成相差一个或若干个CH2原子团的化合物不一定互为同系物
C.所有的烷烃之间一定互为同系物
D.两个相邻同系物的相对分子质量数值一定相差14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种清洁能源.制氢和储氢作为氢能利用的关键技术,是当前科学家主要关注的热点问题.
(1)用甲烷制取氢气的两步反应的能量变化如图所示: 
①甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是 .
②第Ⅱ步反应为可逆反应.800℃时,若CO的起始浓度为2.0molL﹣1 , 水蒸气的起始浓度为3.0molL﹣1 , 达到化学平衡状态后,测得CO2的浓度为1.2molL﹣1 , 则CO的平衡转化率为 .
(2)NaBH4是一种重要的储氢载体,能与水反应生成NaBO2 , 且反应前后B元素的化合价不变,该反应的化学方程式为 , 反应消耗1mol NaBH4时转移的电子数目为 .
(3)储氢还可借助有机物,如利用环已烷和苯之间的可逆反应来实现脱氢和加氢. 
在某温度下,向恒容容器中加入环已烷,其起始浓度为a molL﹣1 , 平衡时苯的浓度为b molL﹣1 , 该反应的平衡常数K=(用含a、b的关系式表达).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com