
����Ŀ�������������������γɵ�����Ĥ��������Ȼ����Ĥ��ĥ�ԡ���ʴ�Լ�װ���������Ե���ߣ���ҵ������Ϊ����������������Һ�е�����Ƶ���������Ĥ��װ����ͼ��ʾ������˵����ȷ����(����)
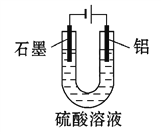
A. �����缫����ʽΪAl-3e-+6OH-Al2O3+H2O
B. ���ŵ��Ľ��У���Һ��pH������
C. ��������������3.36 L(��״��)ʱ����������2.4 g
D. ��������H+�������缫
���𰸡�C
�����������������A�������Ϊ������Һ��OH�����ܲμӷ�Ӧ������B������ԭ���װ�ú���Ŀ��Ϣ��֪����ܷ�ӦΪ��2Al+3H2O![]() Al2O3+3H2����H2O���٣���Һ��pH��С������C��������ӦΪ��2H++2e=H2����H2�����ʵ���Ϊ3.36L��22.4L/mol=0.15mol����ת�Ƶ���Ϊ��2��0.15mol=0.3mol��������ӦΪ�����ݲ��������м��㣺���������ص�����Ϊx��
Al2O3+3H2����H2O���٣���Һ��pH��С������C��������ӦΪ��2H++2e=H2����H2�����ʵ���Ϊ3.36L��22.4L/mol=0.15mol����ת�Ƶ���Ϊ��2��0.15mol=0.3mol��������ӦΪ�����ݲ��������м��㣺���������ص�����Ϊx��
2Al+3H2O-6e=Al2O3+6H+m
6mol 48g
0.3mol x
6mol��0.3mol=48g��x�����x=2.4g������������2.4g����ȷ��D�����ݵ����ķ����֪����������������������H+����ʯī�缫������


 ��ѧ��ʦ����ϵ�д�
��ѧ��ʦ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.ú��������Ϊ����ȼ�ϵĹ������������仯
B.���ۡ���֬�͵����ʶ��Ǹ߷��ӻ�����
C.��ϩ���Ҵ�����ʹ����KMnO4��Һ��ɫ
D.����������ֲ���;���ˮ�������Ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��仯��������ͼ�����б�������ȷ���ǣ� �� 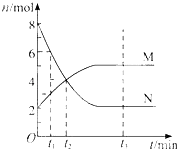
A.��Ӧ�Ļ�ѧ����ʽΪ��2MN
B.t2ʱ�����淴Ӧ������ȣ��ﵽƽ��
C.t3ʱ������Ӧ���ʴ����淴Ӧ����
D.t1ʱ��N��Ũ����MŨ�ȵ�2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£����ݻ��̶���ij�ܱ������з�����ӦN2+3H2![]() 2NH3����10s��N2��Ũ����5 mol��L-1����4 mol��L-1������˵����ȷ����(����)
2NH3����10s��N2��Ũ����5 mol��L-1����4 mol��L-1������˵����ȷ����(����)
A. ��NH3��ʾ�Ļ�ѧ��Ӧ����Ϊ0.1 mol��L-1��s-1
B. ʹ�ú��ʵĴ��������Լӿ�÷�Ӧ������
C. ����H2��Ũ�Ȼ��¶ȶ���ӿ�÷�Ӧ����
D. ��Ӧ�㹻��ʱ�䣬N2��H2��������һ������Ũ�Ƚ�Ϊ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о����������������ڴ����к������ӵ������ʱ���漰���·�Ӧ��
2NO2��g��+NaCl��s��![]() NaNO3��s��+ClNO��g�� K1H < 0��I��
NaNO3��s��+ClNO��g�� K1H < 0��I��
2NO��g��+Cl2��g��![]() 2ClNO��g�� K2H < 0��II��
2ClNO��g�� K2H < 0��II��
��1��4NO2��g��+2NaCl��s��![]() 2NaNO3��s��+2NO��g��+Cl2��g����ƽ�ⳣ��K=_______����K1��K2��ʾ����
2NaNO3��s��+2NO��g��+Cl2��g����ƽ�ⳣ��K=_______����K1��K2��ʾ����
��2��Ϊ�о���ͬ�����Է�Ӧ��II����Ӱ�죬�ں��������£���2L�����ܱ������м���0.2mol NO��0.1mol Cl2��10minʱ��Ӧ��II���ﵽƽ�⡣���10min��v��ClNO��=8.0��10-3molL-1min-1���ش���������
��ƽ���n��Cl2��=__________mol��
��NO��ת���ʧ�1=_______��
�������������ֲ��䣬��Ӧ��II���ں�ѹ�����½��У�ƽ��ʱNO��ת���ʧ�2________��1���>����<����=������ƽ�ⳣ��K2___________���������С�����䡱����
����ҪʹK2��С���ɲ��õĴ�ʩ��________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������Ա�Ϊ��Ҫԭ�ϣ���������·�ߺϳ�����ҩ����������
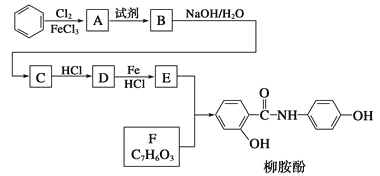
��֪��![]()
�ش��������⣺
��1��д��A��B��Ӧ������Լ�______________��A��B��Ӧ����Ϊ______________________��
��2�����������ӣ�����˵����ȷ����___________��
A.1 mol�����������Ժ�2 molNaOH��Ӧ B. �ɷ���ˮ�ⷴӦ
C. ���ܷ���������Ӧ D.�����巢��ȡ����Ӧ
��3��д��B��C�Ļ�ѧ����ʽ__________________________________��
��4��д��������F�Ľṹ��ʽ_____________________________��
��5��д��ͬʱ��������������F��ͬ���칹��Ľṹ��ʽ________________________��д��3�֣���
�����������ұ����������ֲ�ͬ��ѧ��������ԭ�ӣ� ���ܷ���������Ӧ
��6���Ա�����ϩΪԭ�Ͽɺϳɾ۱���ϩ������ƺϳ�·�ߣ����Լ����ܼ���ѡ����
ע���ϳ�·�ߵ���д��ʽ��������ʾ������ͼ��
![]() ____________________________________��
____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǽ���þ��±�ط�Ӧ�������仯ͼ(��Ӧ����������Ϊ298 Kʱ���ȶ�״̬)������ѡ���в���ȷ����(����)
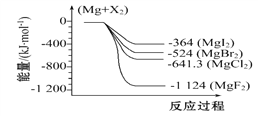
A. Mg��F2��Ӧ����S<0 B. MgF2(s)+Br2(l)MgBr2(s)+F2(g)��H=+600 kJ��mol-1
C. MgBr2��Cl2��Ӧ�Ħ�H<0 D. ����������ȶ�˳��MgI2>MgBr2>MgCl2>MgF2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��С��Ϊ��̽��п�����ᷴӦ�����еĻ�ѧ��Ӧ���ʵı仯����100mLϡ�����м���������п�ۣ���״��������ˮ�������ռ���Ӧ�ų���������ʵ���¼���£��ۼ�ֵ����
ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
���������mL�� | 50 | 120 | 232 | 290 | 310 |
��1����һʱ�����ָ0��1��1��2��2��3��3��4��4��5min����ͬ����Ӧ��������ܵ�ԭ�� ��
��2����һ��ʱ�εķ�Ӧ������С �� ԭ���� ��
��3����2��3����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����Ϊ ��
��4�������Ӧ̫���ң�Ϊ�˼�����Ӧ���ʶ��ֲ����ٲ��������������������зֱ�����������ʣ�
A.����ˮ
B.CH3COONa����
C.Na2CO3��Һ
D.CuSO4��Һ����Ϊ���е��������ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Ͽ���Ƴ�ԭ��صĻ�ѧ��Ӧ�ǣ� ��
A. C(s)+H2O(g)=CO(g)+H2 (g)
B. Ba(OH)28H2O(s)+2NH4C1(s)=BaCl2(aq)+2NH3H2O(l)+8H2O(l)
C. C(s)+CO2(g)=2CO(g)
D. CH4(g)+2O2(g)��CO2(g)+2H2O(l)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com