
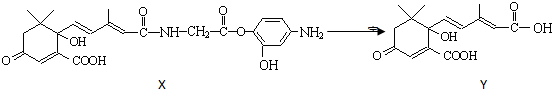
 ( )
( )| A. | Y既可以与FeCl3溶液发生显色反应,又可使酸性KMnO4溶液褪色 | |
| B. | 1 molY与足量NaOH溶液反应,最多消耗3 mol NaOH | |
| C. | 1 molX最多能加成9 molH2 | |
| D. | X可以发生氧化、取代、酯化、加聚、缩聚反应 |
分析 A.Y中含有碳碳双键,但不含酚羟基;
B.Y中只有羧基与氢氧化钠溶液反应;
C.X中能与氢气发生加成反应的碳碳双键、苯环以及1个羰基;
D.X中含有羰基、碳碳双键、羧基、醇羟基、肽键、酯基、酚羟基、氨基,具有酮、烯烃、羧酸、醇、二肽、酯、酚、胺的性质.
解答 解:A.Y中含有碳碳双键,所以能被酸性高锰酸钾溶液氧化,但不含酚羟基,所以不能和氯化铁溶液发生显色反应,故A错误;
B.Y中只有羧基与氢氧化钠溶液反应,含有2个羧基,则最多消耗2 mol NaOH,故B错误;
C.X中能与氢气发生加成反应的碳碳双键、苯环以及1个羰基,则1 molX最多能加成7molH2,故C错误;
D.X中含有羰基、碳碳双键、羧基、醇羟基、肽键、酯基、酚羟基、氨基,具有酮、烯烃、羧酸、醇、二肽、酯、酚、胺的性质,所以能发生氧化、取代、酯化、加聚、缩聚反应,故D正确.
故选D.
点评 本题考查有机物的官能团及其性质,注意有机物的结构和性质的关系,熟悉常见的官能团及醇、烯烃、羧酸、酯的性质即可解答,题目难度不大,选项D为解答的难点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器贮藏贮运浓硫酸 | |
| B. | 氯气具有强氧化性,因此可用于漂白有色布料 | |
| C. | NH3能与Cl2生成NH4Cl,可用浓氨水检验输送氯气的管道是否有泄漏 | |
| D. | 氢氟酸能与二氧化硅反应,因此可用于刻蚀玻璃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 混合液 | A | B | C | D | E | F |
| 4mol•L-1H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为:
).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应为: +(CH3CO)2O$→_{85-90℃}^{浓硫酸}$
+(CH3CO)2O$→_{85-90℃}^{浓硫酸}$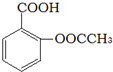 +CH3COOH操作流程如下:
+CH3COOH操作流程如下:
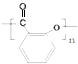 .
.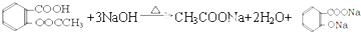 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 正极附近C(H+)逐渐增大 | |
| B. | 正极上产生气泡 | |
| C. | 正极、负极附近C(H+)基本不变 | |
| D. | Zn片、Cu片同时冒出气泡,则说明Zn片不纯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①③④ | B. | ①④ | C. | ②③⑤ | D. | 除② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化亚铁和稀盐酸反应:FeS+2H+=Fe2++H2S↑ | |
| B. | 次氯酸钠溶液中通入少量SO2反应:SO2+H2O+ClO-=SO42-+Cl-+2H+ | |
| C. | 过氧化钠加入足量稀硫酸反应:2Na2O2+4H+═4Na++O2↑+2H2O | |
| D. | 铜粉中加入溴化铁溶液反应:2Fe3++Cu=2Fe2++Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com