
在溶液中能大量共存的离子组是
A.Na+、OH一、HCO3- B.Ba2+、OH一、C1—
C.H+、K+、CO32- D.NH4+、NO3—、OH—
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源:2015-2016学年湖南省高二上第三次月考化学试卷(解析版) 题型:选择题
某温度下,对于反应N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mol。N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是
2NH3(g) ΔH=-92.4kJ/mol。N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是
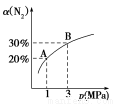
A.将1 mol氮气、3 mol氢气,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ
B.平衡状态由A变到B时,平衡常数K(A)<K(B)
C.上述反应在达到平衡后,增大压强,H2的转化率增大
D.升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
查看答案和解析>>
科目:高中化学 来源:2016届山东省北校高三上学期第二次单元测试化学试卷(解析版) 题型:实验题
(一)如图所示,甲、乙是电化学实验装置,请回答下列问题:
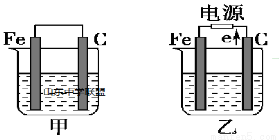
若甲、乙两个烧杯中均盛放饱和NaCl溶液。
①甲中石墨棒上的电极反应式是_________________________________
②乙中总反应的离子方程式为___________________________________
③若乙中含有0.10 mol·L-1NaCl溶液400mL,当阳极产生的气体为560mL(标准状况下)时,溶液的pH=_____________(2分)(假设溶液体积变化忽略不计),转移电子的个数为____________
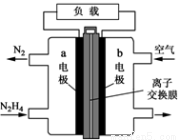
(二)肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景。其工作原理如上图所示,回答下列问题:
①该燃料电池中正极通入的物质是__________;
负极发生的反应式为:__________________________
②电池工作时,OH- 移向极________(“a”或“b”)
③当电池放电转移5mol电子时,至少消耗燃料肼________g
(三)全钒液流电池的结构如图所示,其电解液中含有钒的不同价态的离子、H+和SO42﹣.电池放电时,负极的电极反应为:V2+﹣e﹣=V3+.
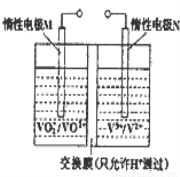
①电池放电时的总反应方程式为___________________________
充电时,电极M应接电源的_________ 极
②若电池初始时左、右两槽内均以VOSO4和H2SO4的混合液为电解液,使用前 需先充电激活,充电过程阴极区的反应分两步完成:第一步VO2+转化为V3+;第二步V3+转化为V2+.则第一步反应过程中阴极区溶液n(H+)_________ _(填“增大”、“不变”或“减小”) (1分),阳极的电极反应式为_________________________
_(填“增大”、“不变”或“减小”) (1分),阳极的电极反应式为_________________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二上学期第一次质检化学试卷(解析版) 题型:选择题
下列热化学方程式正确的是
A.2SO2+O22SO3 ;H =-196.6 kJ·mol-1
B.H2 (g)+1/2O2 (g) = H2O(l);H =-285.8 kJ·mol-1
C.2H2 (g)+O2 (g) = 2H2O(l);H =-571.6 kJ
D.C(s)+O2 (g) = CO2 (g);H = +393.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西省高二上段考文化学试卷(解析版) 题型:选择题
二氧化硫能够使品红溶液褪色,表现了二氧化硫的
A.氧化性 B. 还原性
C.漂白性 D. 酸性氧化物的性质
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上12月月考化学试卷(解析版) 题型:选择题
下列化学用语的描述正确的是( )
A.氨水显碱性:NH3·H2O=NH4+ + OH?
B.硫酸氢钠溶液显酸性:NaHSO4=Na+ + H+ + SO42-
C.Na2S溶液显碱性:S2- + 2H2O  H2S + 2OH-
H2S + 2OH-
D.AlCl3溶液显酸性:Al3+ + 3H2O Al(OH)3↓ + 3H+
Al(OH)3↓ + 3H+
查看答案和解析>>
科目:高中化学 来源:2015-2016年陕西西藏民族学院附属中学高二上期末化学卷(解析版) 题型:选择题
下列有关化学平衡常数K的说法中,正确的是( )
A.K的大小与起始浓度有关
B.温度越高,K值越大
C.K值越大,反应物的转化率越大
D.K值越大,正向反应进行的程度越小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西柳州铁路一中高一上12月月考化学卷(解析版) 题型:选择题
下列实验过程中,始终无明显现象的是( )[来
A.NO2通入FeSO4溶液中 B.CO2通入CaCl2溶液中
C.NH3通入AlCl3溶液中 D.SO2通入已酸化的Ba(NO3)2溶液中
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三上12月月考化学试卷(解析版) 题型:实验题
磷矿石主要以磷酸钙〔Ca3(PO4)2·H2O〕和磷灰石〔Ca5F(PO4)3、Ca5(OH)(PO4)3〕等形式存在。图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸。图(b)是热法磷酸生产过各中由磷灰石制单质磷的流程。


部分物质的相关性质如下:
熔点/℃ | 沸点/℃ | 备注 | |
白磷 | 44 | 280.5 | |
PH3 | -133.8 | -87.8 | 难溶于水,具有还原性 |
SiF4 | -90 | -86 | 易水解 |
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的 %。
(2)以磷灰石为原料,湿法磷酸过程中Ca5F(PO4)3反应的化学方程式为: 。现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得85℅的商品磷酸 吨。
(3)如图(b)所示,热法生产磷酸的第一步是将二氧化硅、过量焦炭与磷灰石混合,高温反应生成白磷。炉渣的主要成分是: (填化学式) ,冷凝塔1的主要沉积物是: 冷凝塔2的主要沉积物是:
(4)尾气中主要含有 ,还含有少量PH3、H2S和HF等,将尾气先通入纯碱溶液,可除去 ;再通入次氯酸钠溶液,可除去 (均填化学式)
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com