
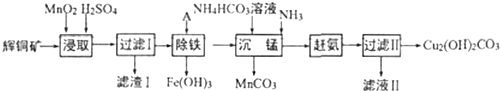
���� ��ͭ����Ҫ�ɷ�ΪCu2S��������Fe2O3��SiO2�����ʣ�����ϡ����Ͷ������̽�ȡ�����˵õ�����ΪMnO2��SiO2������S����Һ�к���Fe3+��Mn2+��Cu2+��������ҺPH��ȥ�����ӣ�����̼�������Һ�����̹��˵õ���Һ�ϳ�����ѭ��ʹ�ã��õ���ʽ̼��ͭ��
��1����߽�ȡ���ʣ�������Ũ�ȡ������¶ȡ�����������������ȣ�
��2������ȡ��ʱ��������������MnO2����Cu2S�õ��������CuSO4��MnSO4��
��3�����ȳ����ٽ�ȡ����ȡ�������Ա�����Fe2O3�ڽ�ȡʱ��ý�����ã�Fe3+�ɴ�Cu2S��MnO2������
��4��������Լ�AӦ���ڵ�����ҺpH���ٽ������ӵ�ˮ�⣬�������������ʣ���ϰ����ӷ����ص������
��5�������̡�����Mn2+�������У�����̼����狀Ͱ���������̼���̳������Դ˿���д��Ӧ�����ӷ���ʽ��
��6����Һ����Ҫ���������Һͨ������Ũ������ȴ�ᾧ������ϴ�ӵõ�����茶��壮
��� �⣺��ͭ����Ҫ�ɷ�ΪCu2S��������Fe2O3��SiO2�����ʣ�����ϡ����Ͷ������̽�ȡ�����˵õ�����ΪMnO2��SiO2������S����Һ�к���Fe3+��Mn2+��Cu2+��������ҺPH��ȥ�����ӣ�����̼�������Һ�����̹��˵õ���Һ�ϳ�����ѭ��ʹ�ã��õ���ʽ̼��ͭ��
��1�����ʱ��ͨ�������ʯ���������¶Ȼ��߽��н��趼������߽�ȡ�ʣ�
�ʴ�Ϊ�������ʯ���ʵ������¶Ȼ���裻
��2������ȡ��ʱ��������������MnO2����Cu2S�õ��������CuSO4��MnSO4���䷴Ӧ�����ӷ���ʽ�ǣ�2MnO2+Cu2S+8H+=S��+2Cu2++2Mn2++4H2O��
�ʴ�Ϊ��2MnO2+Cu2S+8H+=S��+2Cu2++2Mn2++4H2O��
��3����ȡʱ����ͭ��Һϡ����������������ˮ�����ȳ����ٽ�ȡ����ȡ�������Ա�����Fe2O3�ڽ�ȡʱ��ý�����ã�Fe3+�ɴ�Cu2S��MnO2������
�ʴ�Ϊ��Fe3+�ɴ�Cu2S��MnO2������
��4��������Լ�AӦ���ڵ�����ҺpH���ٽ������ӵ�ˮ�⣬�������������ʣ������Ҫ�Ʊ���ʽ̼��ͭ����ɼ�������ͭ��������ͭ�ȣ���ˮ��CaO�������µ����ʣ�
�ʴ�Ϊ��AB��
��5�������̡�����Mn2+�������У�����̼����狀Ͱ���������̼���̳�������Ӧ�����ӷ���ʽΪMn2++HCO3-+NH3=MnCO3��+NH4+��
�ʴ�Ϊ��Mn2++HCO3-+NH3=MnCO3��+NH4+��
��6����Һ����Ҫ���������Һͨ������Ũ������ȴ�ᾧ������ϴ�ӵõ�����茶��壬�ʴ�Ϊ����NH4��2SO4��
���� ���⿼�������ʷ����ᴿ�ķ��������̷���Ӧ�ã�������ѧ���ķ���������ʵ�������Ŀ��飬��������Ŀ��ע�����ʵ��ԭ���Ͳ������̵�Ŀ�ģ���Ҫ���������ʵ����⣬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 CaCl2
CaCl2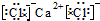 Na2O2
Na2O2 OH-
OH- CH3-
CH3- NaOH
NaOH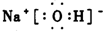
 ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.02mol/��L•s�� | B�� | 1.8mol��L•s�� | C�� | 1.2mol/��L•s�� | D�� | 0.18mol/��L•s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
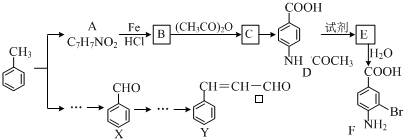
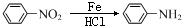
 +��CH3CO��2O��
+��CH3CO��2O��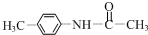 +CH3COOH��
+CH3COOH��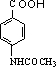 +Br2$\stackrel{Fe}{��}$
+Br2$\stackrel{Fe}{��}$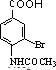 +HBr��
+HBr��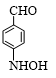 ��
��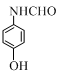 ��
��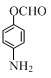 ��
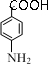
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol ����ϩ�к��е�̼̼˫����Ϊ4NA | |
| B�� | 7.8g�������ƾ����к���0.1NA��O22- | |
| C�� | ��״���£�22.4LNO2�к���NA��NO2���� | |
| D�� | 1 mol•L-1NH4Cl��Һ�У�NH4+��0����ĿС��NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
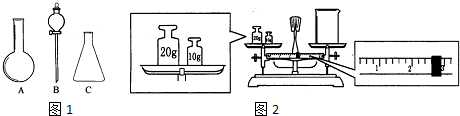

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
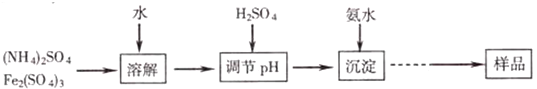
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��b��
��b��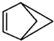 ����ش��������⣺
����ش��������⣺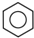 �ṹ��������Щ���治ͬD������ĸ���ţ���
�ṹ��������Щ���治ͬD������ĸ���ţ����鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com