
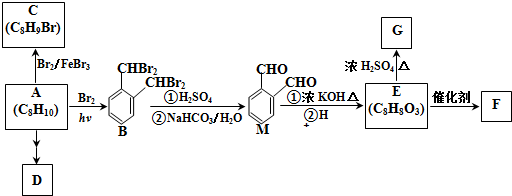

 .由A生成B的反应过程中,会同时生成多种副产物,其中一种与B互为同分异构体,它的核磁共振氢谱有5个吸收峰.
.由A生成B的反应过程中,会同时生成多种副产物,其中一种与B互为同分异构体,它的核磁共振氢谱有5个吸收峰. .
. .
.分析 A和溴发生取代反应生成B,根据B的结构简式知,A的结构简式为 ,A和溴在催化剂条件下发生取代反应生成C,根据C的分子式知,C的结构简式为
,A和溴在催化剂条件下发生取代反应生成C,根据C的分子式知,C的结构简式为 ,B发生一系列反应后生成邻苯二甲醛,结合已知反应信息可知,邻苯二甲醛反应生成E,E的结构简式为
,B发生一系列反应后生成邻苯二甲醛,结合已知反应信息可知,邻苯二甲醛反应生成E,E的结构简式为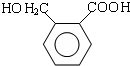 ,E发生缩聚反应生成F,则F的结构简式为
,E发生缩聚反应生成F,则F的结构简式为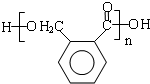 ,G是M同分异构体,E发生分子内酯化反应生成G,G结构简式为
,G是M同分异构体,E发生分子内酯化反应生成G,G结构简式为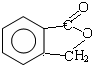 ,
,
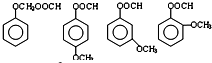
(6)A被酸性高锰酸钾氧化生成二苯甲酸,其结构简式为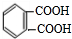 ,邻苯二甲酸与甲醇发生酯化反应酯化反应得到D(邻苯二甲酸二乙酯),据此分析解答.
,邻苯二甲酸与甲醇发生酯化反应酯化反应得到D(邻苯二甲酸二乙酯),据此分析解答.
解答 解:A和溴发生取代反应生成B,根据B的结构简式知,A的结构简式为 ,A和溴在催化剂条件下发生取代反应生成C,根据C的分子式知,C的结构简式为
,A和溴在催化剂条件下发生取代反应生成C,根据C的分子式知,C的结构简式为 ,B发生一系列反应后生成邻苯二甲醛,结合已知反应信息可知,邻苯二甲醛反应生成E,E的结构简式为
,B发生一系列反应后生成邻苯二甲醛,结合已知反应信息可知,邻苯二甲醛反应生成E,E的结构简式为 ,E发生缩聚反应生成F,则F的结构简式为
,E发生缩聚反应生成F,则F的结构简式为 ,G是M同分异构体,E发生分子内酯化反应生成G,G结构简式为
,G是M同分异构体,E发生分子内酯化反应生成G,G结构简式为 ,
,
(1)A为 ,其名称是邻二甲苯,E的结构简式为
,其名称是邻二甲苯,E的结构简式为 ,E中官能团名称是羧基和羟基,
,E中官能团名称是羧基和羟基,
故答案为:邻二甲苯;羧基、羟基;
(2)F结构简式为 ,在该反应的副产物中,与B互为同分异构体的化合物的结构简式为
,在该反应的副产物中,与B互为同分异构体的化合物的结构简式为 ,有5种氢原子,所以其核磁共振氢谱有5个吸收峰,
,有5种氢原子,所以其核磁共振氢谱有5个吸收峰,
故答案为: ;5;
;5;
(3)E发生分子内酯化反应生成G,反应方程式为 ,
,
故答案为: ;
;
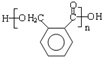
(4)E的同分异构体符合下列条件:
①属于芳香族化合物,说明含有苯环;②分子中含有醚键;③能发生水解反应和银镜反应,说明含有酯基和醛基,则符合条件的同分异构体有 ,所以有4种,
,所以有4种,
故答案为:4; ;
;
(5)C的结构简式为 ,
,
a.溴原子在苯环上,不能够发生消去反应,故错误;
b.可能的结构有2种,故错误;
c.水解产物含有酚羟基,所以能够与FeCl3溶液发生显色反应,故正确;
d.水解生成的酚羟基和HBr都能与NaOH反应,所以1mol的C最多可以和2mol NaOH反应,故正确;
故选cd;
(6)A被酸性高锰酸钾氧化生成二苯甲酸,其结构简式为 ,邻苯二甲酸与甲醇发生酯化反应酯化反应得到D(邻苯二甲酸二乙酯),其合成路线为
,邻苯二甲酸与甲醇发生酯化反应酯化反应得到D(邻苯二甲酸二乙酯),其合成路线为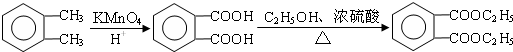 ,故答案为:
,故答案为: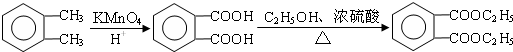 .
.
点评 本题考查有机物推断和合成,为高频考点,侧重考查学生分析判断能力,明确官能团及其性质关系、常见反应类型及反应条件是解本题关键,注意题给信息的灵活运用,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Fe(SO4)2的溶液中:H+、Mg2+、Br-、NO3- | |
| B. | 含有大量HCO3-的溶液:NH4+、Ca2+、AlO2-、I- | |
| C. | 浓度为3%的H2O2溶液:H+、Fe2+、C1-、SO42- | |
| D. | c(S2-)=0.1mo1.L-1的溶液中:Na+、NH4+、ClO-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
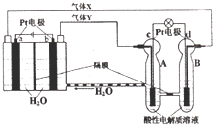
| A. | 有0.1mol电子转移时,a电极产生1.12LO2 | |
| B. | c极上发生还原反应,B中的H+可以通过隔膜进入A | |
| C. | b极上发生的电极反应是:4H2O+4e-=2H2↑+4OH- | |
| D. | d电极上发生的电极反应是:O2+4H++4e-=2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘是人体必需微量元素,所以要多吃富含高碘酸的食物 | |
| B. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| C. | 药皂中含有苯酚,能杀菌消毒,故苯酚具有强氧化性 | |
| D. | 屠呦呦获得了2015年诺贝尔奖,她用乙醚提取青蒿素的过程属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2═Fe+2Li2S.下列说法正确的是( )
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2═Fe+2Li2S.下列说法正确的是( )| A. | Li 发生氧化反应,a 极为阴极 | |
| B. | 电子由 a 极流出通过电流表流入 b 极,然后再由 b 极经内电路回到 a 极 | |
| C. | 可以用水代替 SO(CH3)2做溶剂 | |
| D. | b 极反应式是 FeS2+4Li++4e-═Fe+2Li2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 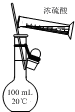 用如图装置配制100 mL 0.1 mol/L的硫酸 | |
| B. |  用如图装置提取碘水中碘 | |
| C. |  用如图装置制取少量乙烯气体 | |
| D. | 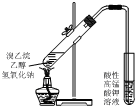 用如图装置验证溴乙烷发生消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
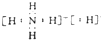 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑦ | B. | ①②⑤⑥ | C. | ③⑤⑥⑦ | D. | ①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com