
 汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体.
汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体.分析 (1)空/燃比较小时,燃料不能充分燃烧,则生成CO;
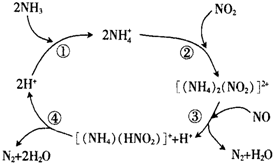
(2)根据图示可知:步骤③反应物为[(NH4)2(NO2)]2+、NO,生成物为N2、H2O、[(NH4)(HNO2)]+、H+,根据原子守恒电荷守恒书写,根据反应①②③④分析可得NH3脱除NO、NO2总反应;
(3)根据题干信息可知反应物为:NaClO2、NO,生成物为:HNO3,结合已知反应方程式进行书写.
解答 解:(1)当空/燃比较小时,汽油中的碳发生不完全燃烧产生一氧化碳,有毒,
故答案为:CO;
(2)根据图示各步反应为:步骤①:NH3+H+=NH4+,步骤②:2NH4++NO2=[(NH4)2(NO2)]2+,步骤③:[(NH4)2(NO2)]2++NO=N2+H2O+[(NH4)(HNO2)]++H+,步骤④:[(NH4)(HNO2)]+=N2+2H2O+H+,①+②+③+④得:NO+NO2+2NH3$\frac{\underline{\;H+\;}}{\;}$2N2+3H2O,所以NH3脱除NO、NO2总反应的化学方程式为:NO+NO2+2NH3$\frac{\underline{\;H+\;}}{\;}$2N2+3H2O,
故答案为:[(NH4)2(NO2)]2++NO=N2+H2O+[(NH4)(HNO2)]++H+;NO+NO2+2NH3$\frac{\underline{\;H+\;}}{\;}$2N2+3H2O;
(3)①NaClO2+HCl=HClO2+NaCl②8HClO2═6ClO2↑+Cl2↑+4H2O③2NaClO2+Cl2═2NaCl+2ClO2↑④5NO+3ClO2+4H2O═5HNO3+3HCl
将$\frac{[①×8+②+③]×3+④×8}{10}$ 得酸性条件下NaClO2溶液将NO转化为HNO3的总反应的化学方程式:3NaClO2+4NO+2H2O═4HNO3+3NaCl,
故答案为:3NaClO2+4NO+2H2O═4HNO3+3NaCl.
点评 本题主要考查了汽车尾气处理,读懂图示以及根据反应物和生成物进行正确书写方程式是解答的关键,题目难度不大.


科目:高中化学 来源: 题型:填空题
| 阳离子 | Na+、Al3+、Ba2+、NH4+ |
| 阴离子 | Cl-、OH-、CO32-、SO42- |
 ,B所含的阳离子的结构示意图是
,B所含的阳离子的结构示意图是 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 2.3 | 4.0 | 7.6 |
| 完全沉淀pH | 4.1 | 5.2 | 9.6 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
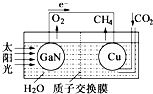 科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以
科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以| A. | 铜电极表面的电极反应式 CO2+8e-+8H+=CH4+2H2O | |
| B. | 为提高该人工光合系统的工作效率,可向装置中加入少量硫酸 | |
| C. | 该装置仅将化学能转变为电能 | |
| D. | 装置中的H+由左向右移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是含有离子键的化合物一定是离子化合物 | |
| B. | 含有共价键的化合物都是共价化合物 | |
| C. | 凡是能电离出离子的化合物都是离子化合物 | |
| D. | 非金属原子间以共价键结合的物质都是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发酵粉中主要含有氢氧化钠,能使焙制出的糕点疏松多孔 | |
| B. | 碘盐中的碘可以直接用淀粉检验 | |
| C. | 碳酸氢钠可用于治疗胃酸过多 | |
| D. | 硫酸氢钠属于盐类,其水溶液显中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
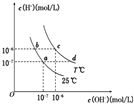 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )| A. | a点对应的溶液中大量存在:CO32-、Na+、Cl-、SO42- | |
| B. | b点对应的溶液中大量存在:Fe2+、Ba2+、K+、NO3- | |
| C. | c点对应的溶液中大量存在:Na+、Ba2+、Cl-、Al3+ | |
| D. | d点对应的溶液中大量存在:Na+、K+、ClO-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 应用高效洁净的能源转换技术,推广使用节能环保材料 | |
| B. | 大力发展火力发电,解决电力紧张问题 | |
| C. | 研发以高纯硅为核心材料的光伏发电技术 | |
| D. | 大力开发新能源,如核能、太阳能、风能等,减少化石能源的使用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com