
【题目】白黎芦醇具有抗氧化和预防心血管疾病的作用。可通过以下方法合成:
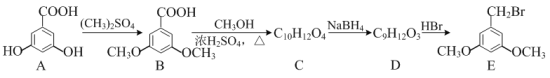

⑴化合物A中所含官能团的名称为______和______。
⑵由F→G的反应类型是______。
⑶D的结构简式为______。
⑷写出同时满足下列条件的C的一种同分异构体的结构简式:______。
①能发生银镜反应,与FeCl3溶液不显色;
②能发生水解反应,水解产物之一能与FeCl3溶液显色;
③分子中含有4种不同化学环境的氢。
⑸请写出以苯甲酸、甲醇为原料制备![]() 的合成路线流程图,无机试剂可任选,合成示例见本题题干。_________________
的合成路线流程图,无机试剂可任选,合成示例见本题题干。_________________
【答案】羧基 羟基 消去反应 
 或
或

【解析】
B发生酯化反应得到C,则C的结构简式为:![]() ,C与硼氢化钠发生还原反应生成D,D与HBr发生取代反应生成E,根据D的分子式和E的结构简式可知D的结构简式为
,C与硼氢化钠发生还原反应生成D,D与HBr发生取代反应生成E,根据D的分子式和E的结构简式可知D的结构简式为 ,E发生加成反应生成F,结合G的分子式推知F在浓硫酸作用下发生了消去反应,生成G的结构简式为:
,E发生加成反应生成F,结合G的分子式推知F在浓硫酸作用下发生了消去反应,生成G的结构简式为:![]() ,G和三溴化硼反应生成白藜芦醇,据此分析作答。
,G和三溴化硼反应生成白藜芦醇,据此分析作答。
⑴化合物A为中所含官能团为羧基和羟基,故答案为:羧基;羟基;
⑵F在浓硫酸作用下发生了消去反应生成G,故答案为:消去反应;
⑶根据上述分析可知,D的结构简式为 ;
;
⑷C为![]() ,分子式为:C10H12O4,不饱和度为
,分子式为:C10H12O4,不饱和度为![]() =5,,①能发生银镜反应,与FeCl3溶液不显色,说明分子内含醛基,不含酚羟基;②能发生水解反应,水解产物之一能与FeCl3溶液显色,说明含有酯基;③分子中含有4种不同化学环境的氢,则符合上述条件的同分异构体为:
=5,,①能发生银镜反应,与FeCl3溶液不显色,说明分子内含醛基,不含酚羟基;②能发生水解反应,水解产物之一能与FeCl3溶液显色,说明含有酯基;③分子中含有4种不同化学环境的氢,则符合上述条件的同分异构体为: 或
或 ;
;
⑸根据给出的合成路线,可知,苯甲酸可先与甲醇发生酯化反应生成苯甲酸甲酯,然后在硼氢化钠作用下发生换换反应生成苯甲醇,再与HBr发生取代反应生成![]() ,同时苯甲醇与氧气发生催化氧化生成苯甲醛,最后根据E到F的合成思路纸杯所需目标产物,具体合成路线 如下:
,同时苯甲醇与氧气发生催化氧化生成苯甲醛,最后根据E到F的合成思路纸杯所需目标产物,具体合成路线 如下: 。
。


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1)写出元素符号和名称:
①________,②________,⑧________,⑨________。
(2)写出下列反应的化学方程式:
⑤的氧化物跟④的氢氧化物溶液反应:________________________________
⑥的单质在③的单质中燃烧:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,既能发生化学反应使溴水褪色,又能使酸性KMnO4溶液褪色的是( )
①SO2 ②CH2=CH2 ③![]() ④CH3CH3
④CH3CH3
A.①②③④B.③④C.①②④D.①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g)==2C(g)+D(g),经2min后B的浓度减少0.6mol·L-1,下列说法正确的是
A. 用A表示的反应速率是0.4mol·L-1·min-1
B. 在2min末的反应速率,用B表示是0.3 mol·L-1·min-1
C. 分别用B、C、D表示反应的速率,其比值是3:2:1
D. 在这2min内B和C两物质浓度是逐渐减小的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的五种前四周期元素。A的核外电子总数与其周期数相同;B的价电子排布式为nsnnpn+2;短周期元素C和D为同周期不相邻的元素,C是同周期元素中离子半径最小的元素,D元素最外层有两个未成对电子;E位于元素周期表的第四周期第IVB族,常用加热ECl4(氯化物)溶液的方法制备纳米材料。回答下列问题:
(1)D元素在周期表中的位置为______,E原子核外有_____个未成对电子,五种元素中电负性最大的是_____(填元素名称)。
(2)由A、B、D三种元素形成的常见三元化合物中具有强氧化性的是______(填化学式)。
(3)氯元素能与C(非碳元素符号)形成某化合物Q。在1.01×105Pa、T1℃时,气体摩尔体积为53.4L/mol,实验测得Q的气态密度为5.00g/L,则此时Q的结构式为___________。(如有配位键须用“→”标出)
(4)A、B、D元素形成的化合物有A2B、DB3,下列关于A2B和DB3的说法中,正确的是________(填标号)。
A.中心原子的价层电子对数目相等 B.都是非极性分子
C.中心原子的孤电子对数目相等 D.都含有极性键
E.都能与Na2O反应 F.固态时晶体类型不同
(5)D在空气中燃烧的产物分子构型为_________。固体DB3中存在如图所示的三聚分子,该分子中D原子的杂化轨道类型为________。

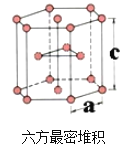
(6)E单质有两种同素异形体,高温下是体心立方堆积;但在常温下的晶体结构为如下图所示的六方最密堆积(底面是正六边形)。已知常温下晶体晶胞参数分别为a cm和c cm,则该晶体的密度可表示为________g·cm-3。(用含a和c的式子表示,用NA表示阿伏伽德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是
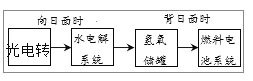
A.该能量转化系统中的水也是可以循环的
B.燃料电池放电时的负极电极反应式:2H2+4OH--4e-=4H2O
C.燃料电池放电时的正极电极反应式:2H2O+O2+4e-=4OH-
D.燃料电池系统产生的能量实际上来自于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: (1)Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
![]() 则
则![]() 的ΔH是( )
的ΔH是( )
A.-824.4 kJmol-1B.-627.6kJmol-1C.-744.7kJmol-1D.-169.4kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁过程中发生的主要反应为:![]() Fe2O3(s) + CO(g)
Fe2O3(s) + CO(g) ![]()
![]() Fe(s) + CO2(g)。已知该反应在不同温度下的平衡常数如下:
Fe(s) + CO2(g)。已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K=_____________,△H________0(填“>”、“<”或“=”)。
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe2O3、CO各1.0 mol,反应经过l0 min后达到平衡。求该时间范围内反应的平均反应速率υ(CO2)=______________________、CO的平衡转化率= _____________。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是_____________。
A.减少Fe的量 B.增加Fe2O3的量 C.移出部分CO2
D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂
(4)在1L的密闭容器中,1300℃条件,下列达平衡状态的是_______________。
A | B | C | D | |
n(Fe2O3) | 0.350 | 0.027 | 0.080 | 0.080 |
n(CO) | 0.010 | 0.010 | 0.010 | 0.050 |
n(Fe) | 0.100 | 0.064 | 0.080 | 0.080 |
n(CO2) | 0.035 | 0.088 | 0.040 | 0.050 |
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关一定物质的量浓度的溶液配制的过程中,造成所得的溶液浓度偏大的是
A.要配制100 mL 1 mol·L-1 NaOH溶液,在白纸上称4 g NaOH固体,并且称量速度较慢
B.定容时俯视容量瓶刻度线
C.溶解或稀释溶质时烧杯尚未干燥
D.定容时盖上瓶盖,摇匀后发现液面低于刻度线,再继续滴加蒸馏水使液面重新达到刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com