
 全部转化成BaSO4沉淀,此时铝元素的存在形式是
全部转化成BaSO4沉淀,此时铝元素的存在形式是A.Al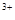 | B.Al(OH)3 | C.AlO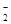 | D.Al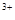 和Al(OH)3 和Al(OH)3 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:实验题
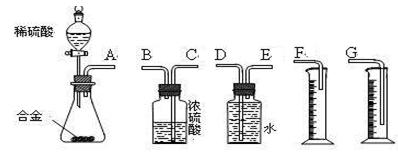
| A.待实验装置冷却后再读数 |
| B.上下移动量筒F,使其中液面与广口瓶中液面相平 |
| C.上下移动量筒G,使其中液面与广口瓶中液面相平 |
| D.视线与凹液面的最低点水平,读取量筒中水的体积 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.都有H2O生成 | B.都有H2生成 | C.都有AlO2—生成 | D.都有Al3+生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3:1 | B.1:3 | C.2:3 | D.3:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.明矾对酸性废水中的悬浮颗粒净化作用较弱 |
| B.用焰色反应检验明矾中的钾离子需用到蓝色钴玻璃 |
| C.向明矾的水溶液中滴加Ba(OH)2溶液,当硫酸根沉淀完全时,所得沉淀的质量最大 |
| D.向明矾的水溶液中滴加Ba(OH)2溶液,开始所得沉淀有两种且两种沉淀物质的量相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④ | B.②③④ | C.①③④ | D.①②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 AlN + CO(配平)
AlN + CO(配平) AlN+3HCl
AlN+3HCl查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com