

 AlN + CO(配平)
AlN + CO(配平) AlN+3HCl
AlN+3HCl 4Al + 3O2↑ 3×104
4Al + 3O2↑ 3×104 4Al + 3O2↑ 中有12个电子转移。
4Al + 3O2↑ 中有12个电子转移。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
 全部转化成BaSO4沉淀,此时铝元素的存在形式是
全部转化成BaSO4沉淀,此时铝元素的存在形式是A.Al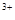 | B.Al(OH)3 | C.AlO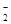 | D.Al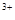 和Al(OH)3 和Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
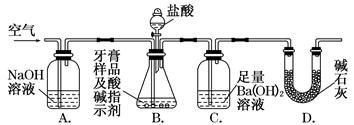
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
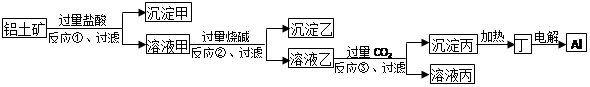
| A.沉淀甲为SiO2 |
| B.生成沉淀乙的反应为:Fe3++3OH-=Fe(OH)3↓ |
| C.溶液乙中含有AlO2- |
| D.反应③为:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
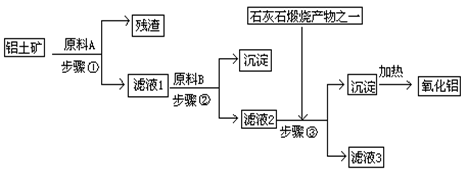
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | -- |
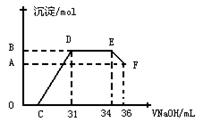
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
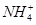 + [AI(OH)4]— ===
+ [AI(OH)4]— ===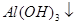
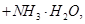 向含有等物质的量的
向含有等物质的量的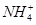 、
、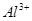 、
、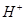 的混合溶液中,慢慢滴加NaOH溶液,直至过量,发生以下离子反应:
的混合溶液中,慢慢滴加NaOH溶液,直至过量,发生以下离子反应: 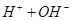 ===
===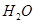 ②
②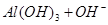 ===[AI(OH)4]—③
===[AI(OH)4]—③ ===
===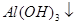
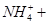
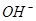 ===
===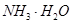 发生反应的先后顺序正确的是
发生反应的先后顺序正确的是A.①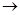 ④ ④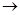 ③ ③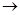 ② ② | B.①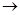 ③ ③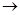 ② ②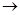 ④ ④ | C.①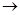 ③ ③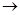 ④ ④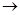 ② ② | D.①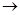 ② ②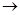 ③ ③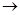 ④ ④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com