


 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案科目:高中化学 来源: 题型:
 密闭容器中mA(g)+nB(g)?pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图.则:
密闭容器中mA(g)+nB(g)?pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图.则:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知某反应A(g)+B(g)?C(g)+D(g) 过程中的能量变化如图所示,回答下列问题:
已知某反应A(g)+B(g)?C(g)+D(g) 过程中的能量变化如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
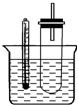 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.查看答案和解析>>
科目:高中化学 来源: 题型:
 为制取较纯净的溴苯和验证反应机理,某化学课外小组设计了实验装置(如图).
为制取较纯净的溴苯和验证反应机理,某化学课外小组设计了实验装置(如图).查看答案和解析>>
科目:高中化学 来源: 题型:
A、1 mol β-紫罗兰酮 与1 mol H2发生加成反应可得到3 种不同产物 与1 mol H2发生加成反应可得到3 种不同产物 |
B、化合物 是苯的同系物 是苯的同系物 |
C、按系统命名法,有机物 可命名为3,7-二甲基-4-乙基辛烷 可命名为3,7-二甲基-4-乙基辛烷 |
D、目前市场上大量矿泉水、食用油等产品包装瓶几乎都是用PET( )的合成单体之一是对苯二甲酸 )的合成单体之一是对苯二甲酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | Si-O | O=O | Si=Si |
| 键能kJ?mol-1 | x | 498.8 | 176 |
| A、460 | B、920 |
| C、1165.2 | D、423.3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com